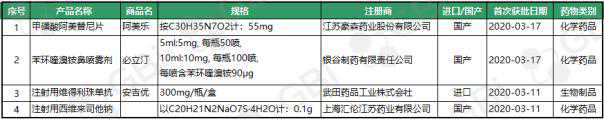
根据GBI来源数据库,2020年3月,中国批准了4种新药(首次在中国上市的分子),包括3种化学药物和1种生物制品。3家获批的化学药品生产企业为:豪森药业、银谷制药、上海汇龙江苏制药,1家获批的生物制品生产企业为武田。
豪森药业:甲磺酸阿美替尼片
3月18日,豪森药业发布公告称,其自主研发的一类创新药甲磺酸阿梅替尼片(商品名:Amerele)已在国家医药产品管理局获批上市,用于治疗“曾接受表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗且T790M突变阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成年患者”。
据悉,阿米乐是继阿斯利康奥昔替尼(商品名泰瑞莎)之后全球第二个三代EGFR-TKI创新药,也是首个国产三代EGFR-TKI创新药。不过,与特蕾莎在国内曾经是一线药物不同,安美乐这次是二线药物获批。不过,豪森表示,根据临床数据,Amerax也是世界上第一个中位无进展生存期(mPFS)超过1年(二线使用)的第三代EGFR-TKI,这也意味着从临床效果来看,它可以作为奥西替尼的二线治疗。为此,业内人士表示,Amerlo上市后将率先对抗Teresha,或将重塑200亿规模的非小细胞肺癌市场格局。
上海交通大学附属胸科医院的路顺教授说,阿米洛利不仅有效,而且安全。该药临床研究中常见的不良反应均可耐受,临床可控在1级或2级。3级及以上不良反应发生率、减少率、中止率低,研究期间无患者发生间质性肺炎。药物相关皮疹、腹泻和QT间期延长的发生率和严重程度较低。目前,Amerlo在全国各大医院和药店均有销售,售价19600元/盒。

另据相关报道,除了已获批的包括奥昔替尼和阿米替尼在内的三代EGFR-TKI药物外,目前国内已有数十家药企布局创新的EGFR-TKI药物,其中已有10余家本土药企进入临床阶段。快消布局包括上海埃利斯研发的阿夫替尼,已于2019年11月29日通过新药上市申请受理,12月纳入优先审评通道。也有望阿夫替尼成为第二个获批的国产第三代EGFR-TKI;另外还有杭州爱森医药研发的阿伐替尼。根据2019年ASCO会议公布的阿伐替尼治疗非小细胞肺癌的II期临床研究结果,在200多名接受阿伐替尼推荐剂量(300mg BID)治疗的受试者中,90%的靶病变明显缩小,ORR为52.2%,DCR为88.0%,中位DOR为7.6个月。
银谷制药:苯环喹溴铵鼻喷雾剂
3月31日,国家美国食品药品监督管理局发布公告,一类创新药物苯环己哌啶鼻喷剂(商品名:必立停)通过优先审评审批程序获准上市,用于改善过敏性鼻炎引起的流涕、鼻塞、鼻痒、打喷嚏等症状。银谷制药有限公司是这种药物的上市许可持有人。
苯并喹诺酮溴化物是一种选择性M胆碱能受体拮抗剂,通过抑制胆碱能神经介导的腺体分泌和炎症反应来缓解过敏性鼻炎症状,具有自主知识产权。银谷制药于2017年11月30日提交上市申请,2018年1月26日,原国家美国食品药品监督管理局公布了银谷制药的苯环喹溴胺等35个药物的临床数据验证。当年1月29日,溴化苯环喹作为“重大项目”进入优先审查。

银谷制药于2007年8月成立于北京中关村海淀园。是一家集创新药物研发、原料药合成、制剂生产、产品销售为一体的创新型制药公司。根据银谷制药R&D中心发布的研究品种,除了新批准的环己基溴化胺鼻腔喷雾剂,YYG
银谷制药在官网显示的上市产品有两种,一种是鲑鱼降钙素注射液(两种规格),主要用于治疗老年骨质疏松症、绝经后骨质疏松症以及骨转移癌引起的高钙血症;另一种是金尔利喷鼻剂(鲑鱼降钙素喷鼻剂),适用于骨质疏松症、伴有骨质溶解和/或骨量减少的骨痛症、佩吉特病(畸形性骨关节炎)、高钙血症和高钙血症危象、神经营养不良症(疼痛性神经营养不良症或苏代克氏病)。
武田:注射用维得利珠单抗
3月12日,五典医药的抗炎新药——注射用韦得珠单抗(商品名:安吉优)获得中国美国食品药品监督管理局批准。批准的适应症是患有中度至重度活动性溃疡性结肠炎和克罗恩病的成年患者,他们对传统治疗或肿瘤坏死因子(TNF)抑制剂的反应不足、无反应或不耐受。2018年,Vedrizumab进入《第一批临床急需境外新药》名单,此次获批成为我国第27个批准上市的临床急需新药。
武田研发的人源化单克隆抗体Vedelizumab,特异性结合47整合素,阻断47与黏膜地址细胞黏附分子-1的结合,从而阻止淋巴细胞进入肠黏膜,有效减轻肠道炎症反应。其中,细胞表面带有整合素47的淋巴细胞特异性地前往肠道组织,这也使得Vituzumab不会影响其他组织器官的免疫功能和炎症反应。
Verlizumab是第一个也是唯一一个专门针对肠道炎症信号通路的药物。其静脉注射剂型于2014年5月在美国和欧盟获得批准。至今已在全球60多个国家和地区获批,用于治疗传统疗法或TNF拮抗剂疗法未充分缓解、不再缓解或不耐受的中重度UC和克罗恩病(CD)患者。
在2019年3月举行的第14届欧洲克罗恩病和结肠炎组织会议上,Takeda宣布了第一个评估vedolizumab治疗中重度UC的头对头IIIb期研究团队的结果。结果显示,在第52周,与阿达木单抗(商品名:Xiumeile)组相比,Vedrizumab组中更高比例的患者实现了临床缓解(31.3% [n=120/383]对22.5% [n=87/386],p=0.0061)和粘膜愈合(39.7)
上海汇龙江苏制药有限公司:注射用西维司他钠。
3月11日,上海汇龙江苏制药有限公司的仿制药塞维司他钠获得国家美国食品药品监督管理局批准上市。其适应症为急性肺损伤(ALI)/急性呼吸窘迫综合征(ARDS),用于改善全身炎症反应综合征。根据CDE的数据,西弗勒斯钠的上市申请是在2月14日提交的,仅用了26天就获得了批准。
天仙钠最初由小叶制药有限公司研制,是弹性蛋白酶(NE)的竞争性抑制剂,可调节急性肺损伤的发病机制。该药物于2002年在日本获准上市,是全球唯一获准用于治疗急性肺损伤的药物。2003年非典爆发时,Severstal作为治疗非典的候选药物,很快被NMPA批准,成为第一个治疗非典的临床药物。
2014年,上海汇龙第一次递交申请。但在2015年“722临床验证风暴”的压力下,数千个药品注册主动撤回上市申请,其中就包括上海汇龙的塞维斯塔钠。今年新型冠状病毒爆发后,在美国食品药品监督管理局紧急药物审批机制下,西维司他钠终于获批上市。