这几年无论是“一致性评价”还是“47”带量采购,我们国家做大做强仿制药的决心超级坚定!通过多项政策的颁布和实施,督促企业进一步客观、切实地控制仿制药的质量和价格,药品监管部门也在努力平衡上市品种的分布,以满足临床需求。今天要说的这个品种的话,抗艾滋病毒药物~阿扎那韦,全球销量一鸣惊人,有明显的治疗作用,但是直到今天,在中国还没有注册!
1.药审中心CDE~通知引导
不久前,CDE发行了《第二批专利权到期、终止、无效且尚无仿制申请的药品清单》,公布了七个品种。“到2018年10月,国内化合物专利权过期、终止、无效且无仿制申请的国外已上市并具有明确临床价值”。其中,用于治疗和预防艾滋病的抗艾滋病病毒药物——中国复方硫酸阿扎那韦的专利于2017年4月14日到期,中国复方专利号为CN1082508C;列在品种表第一位,没有申请注册,值得关注。

图1: 《第二批专利权到期、终止、无效且尚无仿制申请的药品清单》通知
2.药物信息简介
AtazanavirSulfate是一种HIV-1蛋白酶抑制剂,与其他抗逆转录病毒药物联合使用,用于治疗HIV-1感染。它由瑞士诺华公司开发,然后授权给BMS。它于2003年6月获得FDA批准,2003年12月获得PMDA批准,2004年3月获得欧洲EMA批准,商品名为Reyataz。剂型为口服胶囊,有150毫克、200毫克或300毫克三种规格。
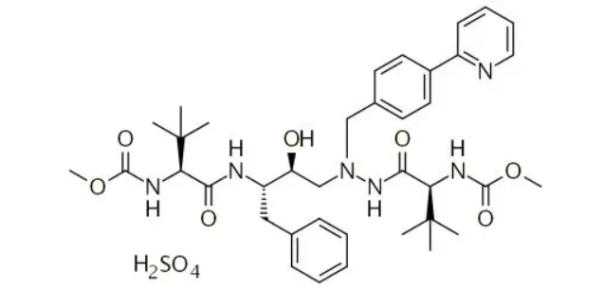
图2:硫酸阿扎那韦的化学结构
3.全球销售数据统计
从全球销售数据来看,硫酸阿扎那韦可以算是一款重磅炸弹药。2007年,其销售额超过10亿美元。但历年来,整体销售数据趋于10亿-20亿美元之间,峰值在15亿美元左右波动,无明显增长趋势。详见下图。
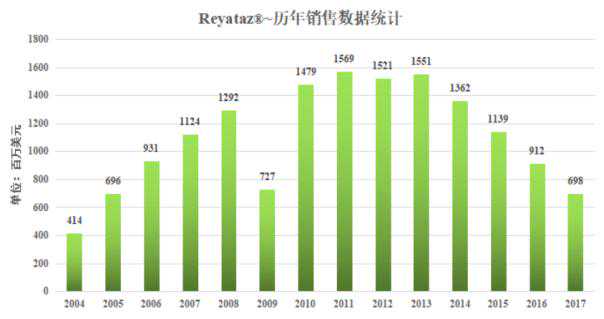
图3: Reyataz ~历年销售数据统计
4.国内注册信息
最初在美国注册上市的硫酸阿扎那韦,在中国已经批准进口。最早承诺日期为2004年12月,申报企业为“百时美施贵宝(中国)投资有限公司”,2005年5月获准进口;然后,他们分别在2010年、2012年、2013年申请了补充;到目前为止,国内还没有该品种的注册仿制企业。
表1:硫酸阿扎那韦的国内注册和申报

5.合成信息
自从它上市以来,许多专利和文献都报道了硫酸阿扎那韦的合成。其中,以下合成路线的批量收率报道为千克,可供参考。
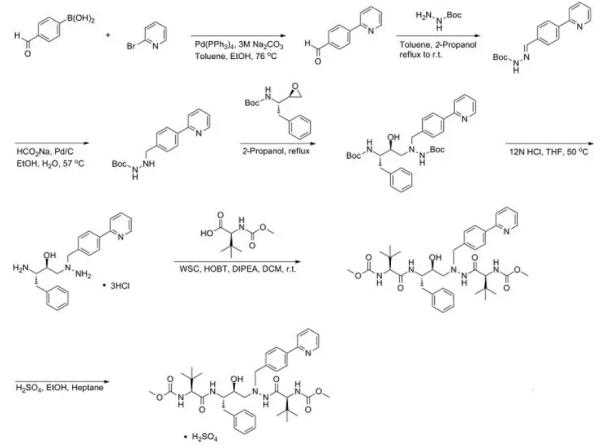
图4:硫酸阿扎那韦(合成路线之一)
6.同类药物总体发展情况
自1995年以来,药物沙奎那韦被FDA批准上市,许多HIV-1蛋白酶抑制剂已被用于临床。从结构上来说,除了替普拉那韦是非肽模拟物,其余都是肽模拟蛋白酶抑制剂。
2000年以前上市的HIV-1蛋白酶抑制剂,通常称为第一代HIV-1蛋白酶抑制剂,在治疗艾滋病方面取得了一定的效果,但由于病毒耐药性和药物本身生物利用度低的特点,逐渐退出市场。
2000年以后上市的HIV-1蛋白酶抑制剂,通常称为第二代HIV-1蛋白酶抑制剂,对临床上已发现的大多数耐药突变株具有良好的抑制活性,其耐药性和生物利用度较第一代抑制剂有显著提高。结构信息见下图。
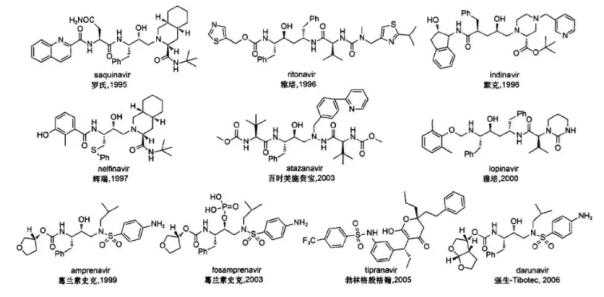
图5:列出的HIV-1蛋白酶抑制剂
7.同类药物国内注册情况
通过逐一查询,国内药企为上述HIV-1蛋白酶抑制剂的仿制注册了大量品种为茚地那韦;获得该品种生产批文的企业有浙江华海、厦门迈克、河南田放、东北制药、齐鲁制药。总体承办日期和办理情况见下图。
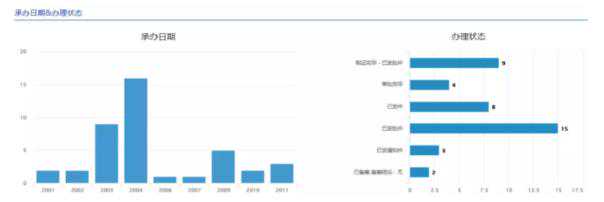
图indinavir ~国内注册申报。
8.小结
通过以上查询发现,国内企业对HIV-1蛋白酶抑制剂的仿制开发相对于肿瘤、内分泌等领域来说是比较低的。除原研外,国内注册申报企业“少而集中”!CDE 《第二批专利权到期、终止、无效且尚无仿制申请的药品清单》公布的七个品种之一,另一种HIV-1蛋白酶抑制剂,地拉那韦,也是其中之一。虽然国内药企对这类药物的创新和仿制热情相对较低,但现实情况是我国艾滋病患者与日俱增..................