多形性胶质母细胞瘤(GBM)是星形细胞瘤中恶性程度最高的一种,但至今仍未找到有效的治疗方法。病人通常在确诊后两年内死亡。这种疾病之所以难以治疗,很大程度上是因为肿瘤包含许多不同的细胞,其侵袭性在患者之间差异很大。
胶质母细胞瘤为什么这么难治疗?为什么传统疗法对它不起作用?还是单病种?这些问题不仅让科学家深感困惑,也让临床医生对患者束手无策。
发表在最新一期《Cell》杂志封面上的一项研究可能会给出答案。麻省总医院(MGH)和布罗德研究所的Cyril Neftel博士领导的实验结果表明,胶质细胞的四种亚型可以通过单细胞测序进行随机切换,这就是为什么癌细胞很难用药物杀死。这一发现将有助于开发更好的胶质母细胞瘤治疗方法。
DOI:https :///10.1016/
确定:肿瘤的四种亚型
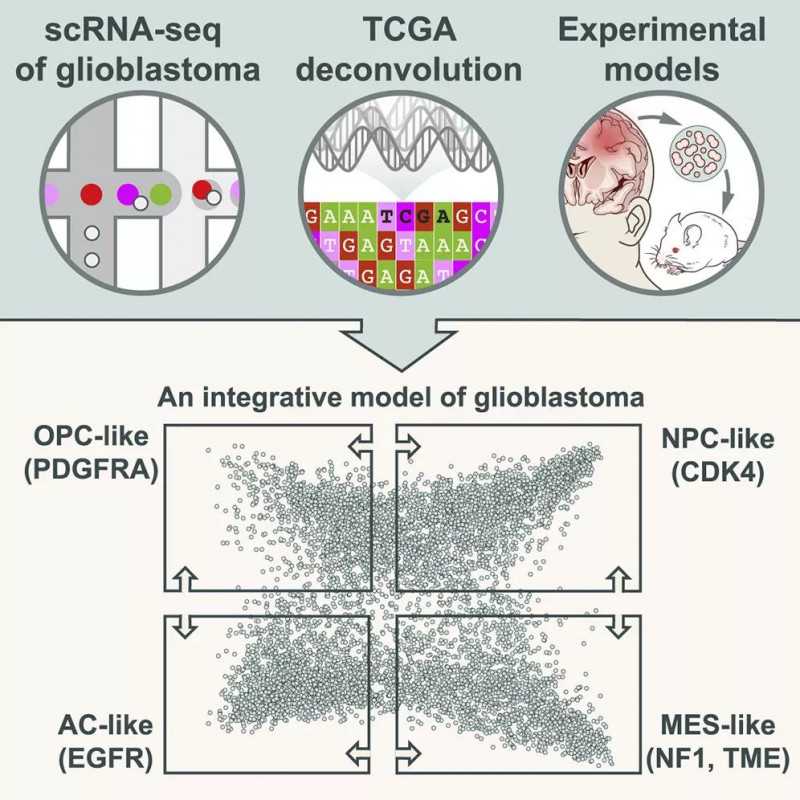
2010年,杰克逊基因组医学实验室的Roel Verhaak教授在《Cancer Cell》期刊上发表了一篇具有里程碑意义的论文,首次根据患者肿瘤的分子标准将胶质母细胞瘤分为四种亚型:神经祖细胞、少突胶质祖细胞、星形胶质细胞和间充质细胞,为胶质母细胞瘤的研究提供了新的视角。
DOI:
随后的研究进一步表明,每种亚型不仅有其独特的基因表达,而且胶质母细胞瘤的组成总是由一种以上的亚型组成,组合亚型的比例可能随时间和治疗而变化。
这些研究为胶质母细胞瘤的研究绘制了一个总体框架,但由于这些研究都专注于大量来自肿瘤细胞的遗传物质样本,这些样本已经被组合和测序,因此它们仍然没有提供更详细的细节供临床医学参考。
测定:四种亚型的基因表达
因此,为了更好地了解这四种亚型在肿瘤细胞中的比例与胶质母细胞瘤状态之间的关系,研究人员决定使用单细胞RNA测序技术来揭示单个细胞的基因表达。
Suv是Broad表观基因组计划的成员,也是MGH病理学系的分子病理学家,他说:“这是迄今为止最大的胶质母细胞瘤单细胞测序研究。我们将个体细胞状态及其相关的基因变化置于其发育背景中,试图了解哪些细胞类型正在驱动疾病。”
研究人员从20名成人和8名儿童胶质母细胞瘤患者中选择了总共24131个肿瘤细胞进行测序,并在癌症基因组图谱(TCGA)的背景下描述了401个胶质母细胞瘤细胞的启动子DNA甲基化变化。
研究人员发现,与前面描述的胶质母细胞瘤的四种亚型相关,细胞中有四种不同的基因表达程序,代表四种不同的细胞状态:神经祖细胞样、少突胶质细胞样祖细胞样、类星体细胞样和间充质样。虽然表达这四种状态的细胞在某种程度上与正常的脑细胞类型相似,但它们的本质有着重要的差异,使细胞癌变。
是什么导致这些细胞癌变?在进一步的研究中,研究人员从遗传基因和肿瘤微环境入手,寻找在特定细胞状态下能够导致细胞癌变的相关基因。他们发现CDK4、EGFR和PDGFRA位点和NF1位点的突变是胶质母细胞瘤的常见遗传驱动因素,在肿瘤细胞的状态表达和决定有多少细胞处于这种状态中起着关键作用,而肿瘤微环境在间充质样状态的表达中也起着重要作用。
突破:四种状态随意切换
研究人员观察到,尽管大多数细胞清楚地将自己识别为四种亚型中的一种,但其中约有15%的细胞同时表达两种亚型的细胞状态。为了检验这一观察结果,研究人员给小鼠注射了只表达一种人源的胶质母细胞瘤细胞,以观察小鼠肿瘤状态的变化。
研究人员从具有四种细胞状态的胶质母细胞瘤中提取了单个星形胶质细胞样细胞,并将其注射到小鼠体内。随着时间的推移,肿瘤逐渐增大。观察到小鼠的肿瘤细胞不仅含有星形胶质细胞样状态,还含有其他三种细胞状态,比例与提取前细胞大致相同。这表明胶质母细胞瘤细胞可以从一种状态变为任何状态。
在使用基因测序跟踪小鼠胶质母细胞瘤模型和携带人类胶质母细胞瘤细胞的小鼠中单个细胞如何发展和变化后,该团队得出了相同的结论。
Mariella G. Filbin博士说:肿瘤很容易随意变成别的东西来躲避我们的药物治疗,这也可以解释为什么单靶点药物在胶质母细胞瘤的治疗中会失败!
联合治疗:未来治疗方向
苏瓦博士也对这些研究成果进行了评价:如果你知道这是一种由多种状态驱动的疾病,每种疾病都有相应的癌症基因,你就会更清楚为什么一个基因至今失效。这些发现为为什么现有的癌症治疗不能阻止胶质母细胞瘤的生长提供了线索。
研究人员目前正在开发一种同时针对所有四种肿瘤状态的联合疗法。菲尔宾博士和他的同事正计划尝试使用基因编辑和药物组合来改变细胞状态。他们希望这些药物可以阻断使肿瘤细胞不成熟的分子通路,或者将DNA包装到染色质中,以决定RNA转录。
菲尔宾博士说:“将新技术应用于这些恶性肿瘤,让我们有机会从几年前无法想象的全新层面了解它们的驱动力。现在是时候将这些研究成果转化为新的疗法了。”
[1]胶质母细胞瘤的细胞状态、可塑性和遗传学的综合模型
[2]单细胞测序揭示胶质母细胞瘤的变形本质
[3]研究暗示了为什么侵袭性脑癌难以治疗