2016年5月31日,国家卫生计生委发布第一批鼓励R&D申报的儿童用药目录,共32个品种(以上市行数计,下同);时隔一年,卫生计生委再次公示第二批儿童用药鼓励R&D申报推荐名单,共40个品种。
根据申报批准挑选品种
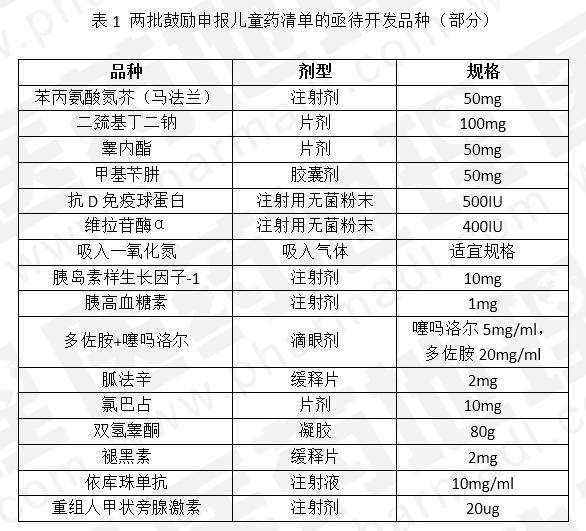
在上述两批72个品种中,经进一步筛选,有9个品种在国内既未申报也未上市,10个品种仅在CDE申报但尚未上市;如果加上剂型,尚未上市的10个CDE品种中有3个品种的剂型从未申报过。这些品种正等着各个企业“认领”。
根据市场表现布局品种
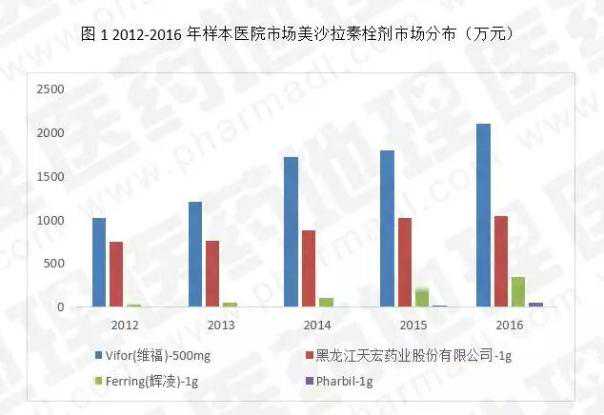
基于PDB样本医院药品数据库,上述两批72个品种中,有49个纳入数据库,其中12个符合剂型条件,3个品种也符合规格条件。比如美沙拉秦栓剂的市场在2012-2016年一直保持稳定增长,尤其是500mg规格的Vifor公司,近年来在该细分市场排名第一。鼓励申报的相关政策出台,会让更多国内企业愿意加入500mg市场,而不是1g市场。
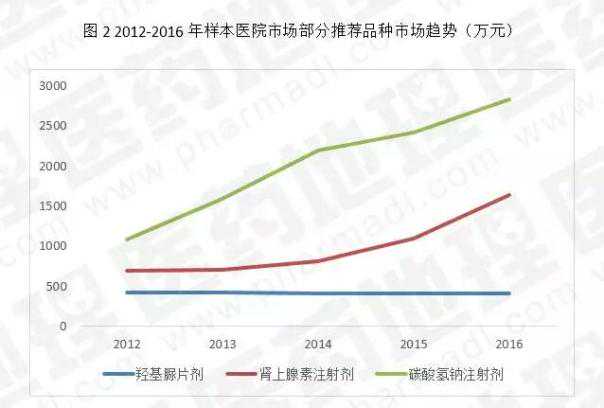
另一方面,在符合剂型条件的12个品种中,选择抗肿瘤、心血管和血液系统的3个品种。可以看出,后两个品种在2012-2106年发展较好,其现有的规格也相当多,尤其是碳酸氢钠,可以作为静脉输液,有10多个规格。这次推荐的新规格可能不会对市场产生太大影响。而近两年略有下滑的羟基脲片现在是市场主流,推荐的500mg规格会在一定程度上促进这一细分市场。
根据剂型领域推算品种
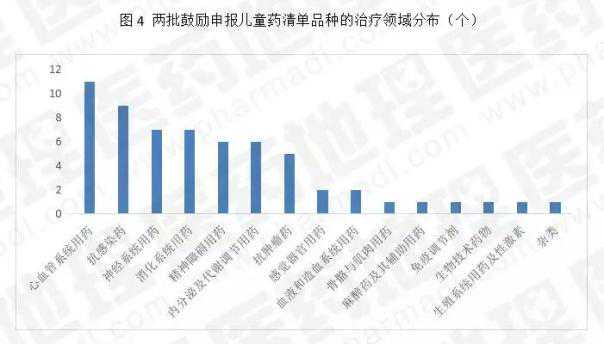
在上述两个批次的72个品种中,统计了剂型分布情况。注射剂占27.78%,居首位,其次是溶液剂和片剂。按照给药途径,口服品种比例将达到60%以上,其中口服液体制剂占2/3以上。
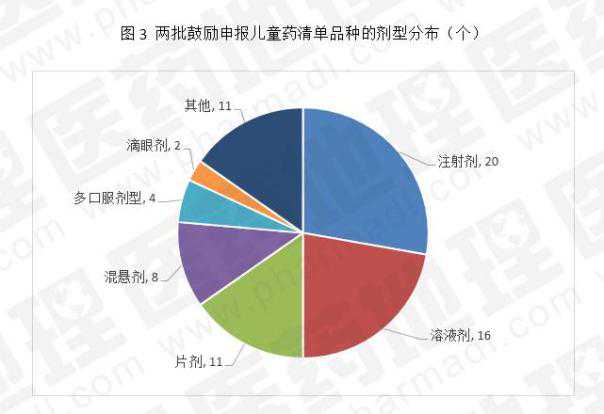
基于PDB数据,在上述两批共72个品种中,剔除了9个既未申报也未上市的品种,统计了其处理场的分布情况。儿科常用抗感染药物数量位居第二,占14.75%,神经系统和消化系统并列第三。此外,没有各种呼吸系统或相关剂型。