近日,由南开大学陈悦教授攻关8年的抗胶质瘤药物ACT001获得FDA罕见病药物(即孤儿药)认证,成为国内为数不多获得认证的药物。Insight数据库显示,该药已在中国获得临床批准。

看到这个新闻,尹爵士很好奇,这些药物在中国最高R&D阶段是什么,获得了FDA孤儿药资格?他们中有多少人有医疗保险?国内药企创新孤儿药研发进展如何?
Insight数据显示,目前有286种药物(以药物主要成分计算)被FDA认证为孤儿药,在CFDA有报告。在这里,我们将从数据层面对这些药物做一个报告。
FDA 孤儿药在国内的最高研发阶段
1. 已上市
据Insight统计,已有195种FDA认可的孤儿药在中国上市。根据全球500种孤儿药的数据,相当于60%的孤儿药还没有推出。
要公示的数据太多了。如需下载上市195孤儿药数据表,请加我微信(yiyaoshujuku001)哈~
在这些上市的孤儿药中,2017年有129个孤儿药纳入医保,其中包括8个通过谈判进入医保的药品,如下图所示:
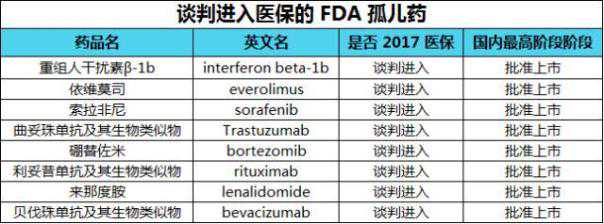
2. 上市申请中
目前有14种药物处于上市申请阶段,如下图所示:
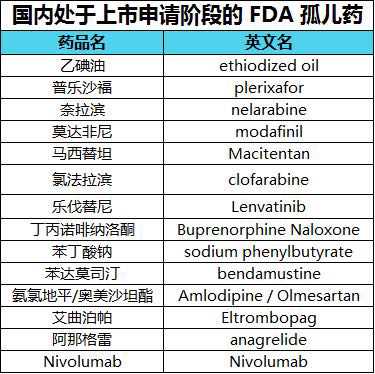
其中,蒂瓦药业的抗癌药苯达莫司汀于2013年11月27日获得FDA孤儿药资格。孤儿药标签用于苯达莫司汀治疗无痛性B细胞非霍奇金淋巴瘤(iNHL)。它适用于在利妥昔单抗或含利妥昔单抗治疗方案治疗期间或6个月内iNHL进展的患者。目前国内上市公司有4家,如下图所示。
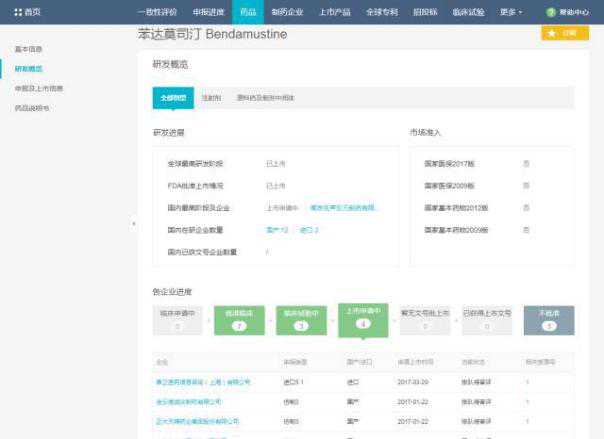
3. 临床试验中
目前共有28种药物处于临床试验阶段,如下图所示:
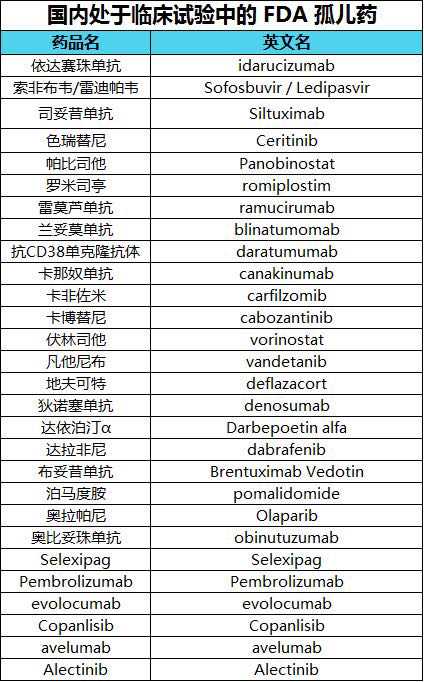
4. 获批临床(临床试验暂未开始)
目前,共有33种药物处于批准的临床阶段,但尚未开始临床试验,如下图所示:
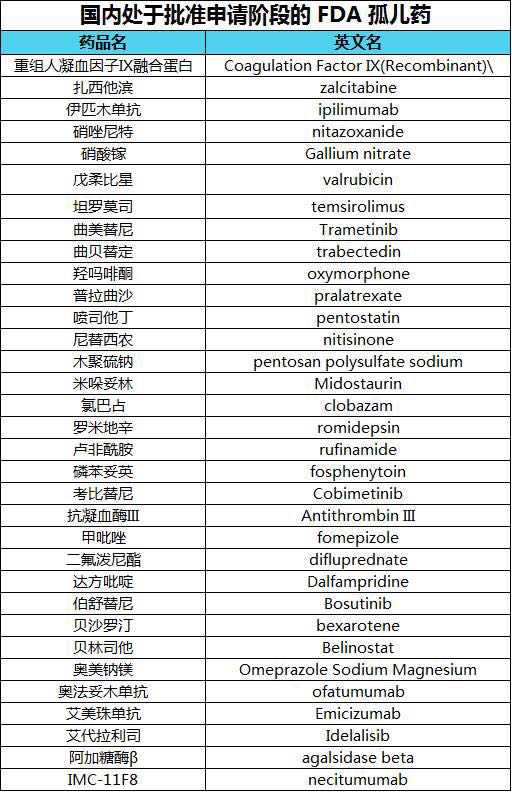
5. 申请临床中
目前有10种药物处于临床试验应用阶段,如下图所示:
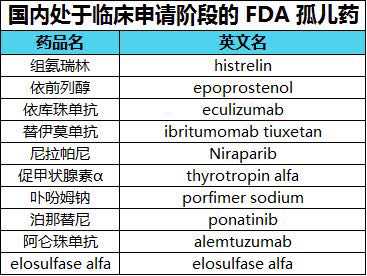
6. 未批准
目前共有5个药物处于批准的临床试验阶段,具体如下图所示:
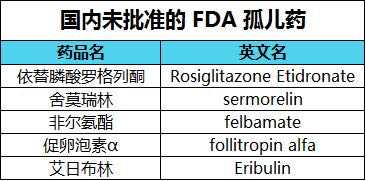
孤儿药上市走绿色通道
近年来,国家出台了一系列扶持孤儿药的药品政策,包括加快审批、单独排队、全球临床试验互认、临床试验豁免等。
例如,在税务总局关于征求意见的最新公告(2017年第52号)《关于鼓励药品医疗器械创新加快新药医疗器械上市审评审批的相关政策》(征求意见稿):
支持罕见病治疗药物和医疗器械的研发。罕见病目录由卫生计生部门公布,建立罕见病患者登记制度。罕见病药品和医疗器械申请人可申请临床试验减免,加快罕见病医疗器械审评审批。对于国外已经批准上市的罕见病治疗药物和医疗器械,可以有条件批准上市,上市后在规定时间内做好相关研究。
第55号通知指出:
对既是创新药又是罕见病的药品,给予10年数据保护期;对属于改良新药的稀有药物给予3年的数据保护期,以鼓励药企有更多的R&D动力。
孤儿药,中国造
在国家鼓励政策的支持下,本土企业也纷纷涉足孤儿药的研发领域。CDE 2017年称,根据Insight统计,19种稀有药物被纳入优先审评。