FDA警告信由美国美国食品药品监督管理局(FDA)向企业或个人发出。这是第一个官方通知,他们的产品,生产,经营或其他活动违反了美国现行的《食品、药品和化妆品法案》。警告信是在FDA高层的批准下发出的,这是权威的。理解这样一份重量级的文件,对一个企业的发展至关重要。从宏观角度看,了解警示函的内容,可以帮助我们了解国际医药行业产品质量控制的趋势和共性问题。从微观上看,可以从FDA的监管重点、意图和现场操作中发现企业质量管理体系存在的问题或改进方向。
本文为大家总结了2016年FDA警告信。这些信息足以帮助GMP审核员和QA人员评估公司的合规水平或发现相应的不足。我们通过数据和图表对预警原因、公司名称、公司所属国家进行了总结和梳理。
表1列出了警告信的发布日期、公司名称和公司所属国家。前两次预警事件发生在2015年,但直到2016年才公布。
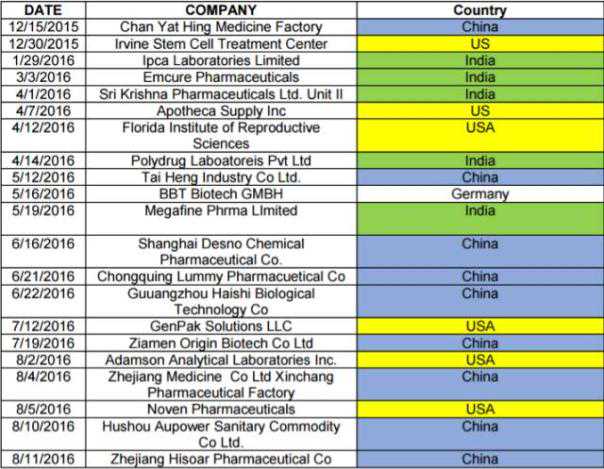
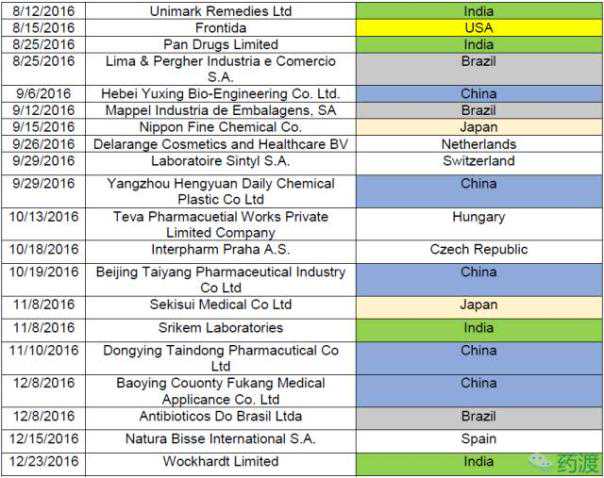
表2列出了2015年和2016年收到FDA警告信的公司所在国家,以及统计的次数。相比2015年的2起,2016年中国企业收到14起FDA警告,位居第一。印度排名第一,2015年有10起,2016年有9起。
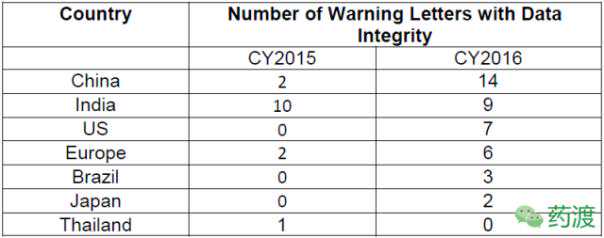
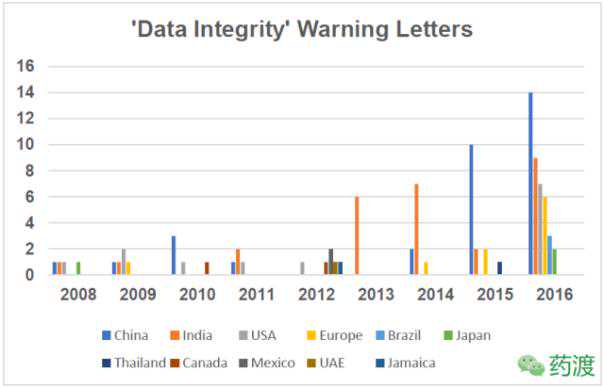
图1统计了2008年至2016年因缺乏数据完整性而被FDA警告的公司所在国家,以及该国收到的警告信总数。有些国家常年上榜,包括美国、中国、印度、欧洲。而美国在2013年、2014年和2015年都没有收到数据完整性丧失的警告信,但在2016年却跃升至第三位。
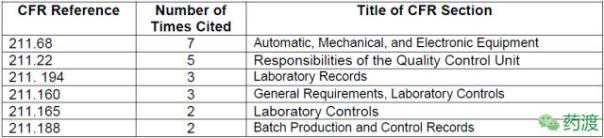
3表3列出了2016年FDA警告信涉及的管理和规则的具体内容,主要包括自动化、机械、电子设备、质量控制、实验室记录、总则、生产等方面。表4综合统计了2008年至2014年FDA警告信中涉及管理和法规具体内容的频率。
总结
1.从监管机构的角度来看,健康的权威监管和正确的政策引导对行业发展的积极影响远大于为检而检。
2.站在企业的角度,虽然亡羊补牢为时未晚,但毕竟羊死了。的确,整治需要大量的时间、精力和财力,尤其是购买新的软件和设备。但是,如果一个企业能够主动改进生产流程,而不是被动地接受检查,通过资源的合理配置,做好短期和长期的规划,那么不仅实现了企业的利益,也促进了行业的发展。
3.说到底,市场是政府、企业和消费者博弈的地方。我们希望看到资源在这三方之间合理分配,这样整个市场才能正常成长。
参考