在一项新的研究中,来自Dana Farber癌症研究所、波士顿儿童医院和麻省大学医学院的研究人员开发了一种治疗镰状细胞病(最常见的遗传性血液疾病)的策略,方法是将CRISPR-Cas9基因编辑应用于患者自身的造血干细胞。这种方法克服了以前的技术挑战,比过去更有效地编辑造血干细胞。相关研究成果于2019年3月25日在线发表在《自然医学》杂志上,题目为《人类造血干细胞高效治疗性基因编辑》。论文作者为丹尼尔鲍尔博士,论文第一作者为吴宇轩和曾静。
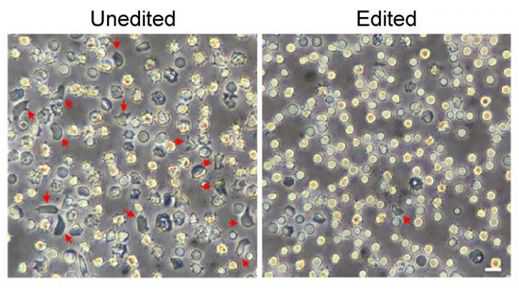
图片来自丹尼尔鲍尔/波士顿儿童医院。
这项新研究发现,这些基因编辑的造血干细胞产生了基因修正的红细胞,从而产生了功能性血红蛋白。
鲍尔说,“我们认为我们的研究已经确定了一种可能治愈常见血红蛋白疾病的策略。将基因编辑与自体干细胞移植相结合,可能是一种治疗镰状细胞病、-地中海贫血和其他血液疾病的方法。”
根据世界卫生组织(世卫组织)的统计,镰状细胞病和-地中海贫血每年影响全球332,000名孕妇或产妇。这两种疾病都涉及编码珠蛋白的基因突变。在-地中海贫血中,突变会阻止红细胞产生足够的携氧血红蛋白分子,从而导致贫血。在镰状细胞病中,突变导致血红蛋白改变形状,使红细胞变形为僵硬的“镰刀”状,从而堵塞血管。
在这项新的研究中,使用了CRISPR-Cas9技术,特别是由麻省大学医学院的Scot Wolfe博士领导的研究团队对Cas9蛋白进行基因修饰,以优化基因编辑。在以前尝试编辑人工血干/祖细胞基因组的过程中,一旦这些基因编辑的细胞被植入骨髓,基因编辑的效率、特异性和长期稳定性都会发生变化。这项新技术提高了基因编辑的针对性和持久性。
Wolfe说,“高效编辑造血干细胞群体——理想情况下接近100%——对于在患者身上实现持久的治疗效果至关重要。通过科学界许多实验室的贡献,朝着这一目标取得了进展。我的研究团队与鲍尔实验室合作,致力于提高CRISPR-Cas9技术进入细胞核的输送和进入效率,从而实现对整个造血干细胞群体近乎完整的治疗性编辑。”
鲍尔的团队使用这种策略进行高度针对性的基因编辑。波士顿儿童医院之前的研究表明,使一种叫做BCL11A的基因失活,可以让红细胞即使在出生后也能继续产生胎儿血红蛋白。胎儿血红蛋白不产生镰刀形,可以替代有缺陷的“成人”血红蛋白。最近,鲍尔发现了一个更安全的靶点:bcl-11a基因的增强子,它只在红细胞中有活性。
鲍尔说,“通过使用我们开发的这种新的非常有效的方法,我们可以在我们收集的几乎所有造血干细胞中编辑BCL11A的增强子,从而克服这些细胞的基因编辑所面临的一些技术挑战。在我们的实验中,超过95%的增强子序列拷贝在我们预期的治疗中发生了变化。”
这种策略使携带镰状细胞病患者造血干细胞的小鼠产生具有足够胎儿血红蛋白的红细胞,从而防止红细胞产生镰状。鲍尔的团队发现,这些基因编辑的造血干细胞在移植到骨髓后,产生了基因修正的红细胞。随后,当从这些小鼠中分离出造血干细胞并移植到其他小鼠中时,这些造血干细胞再次被建群,并且仍然携带治疗性基因改变。
当这种策略应用于来自-地中海贫血患者的造血干细胞时,它恢复了构成血红蛋白的珠蛋白链的正常平衡。
为临床试验做准备
这些研究人员正在采取措施,将他们开发的BCL11A增强子编辑策略应用于临床。他们正在开发临床级的大规模细胞产品制造方案,并进行获得美国美国食品药品监督管理局(FDA)批准所需的安全性研究。他们计划向美国心肺血液研究所镰状细胞病治疗项目寻求资金支持,以便在患者中进行临床试验。
波士顿儿童医院的Dana Farber癌症研究所/癌症血液疾病中心已经开始了镰状细胞病基因治疗的临床试验。方法将患者造血干细胞暴露于携带说明书的慢病毒中,抑制红细胞前体细胞bcl-11a基因的表达,从而增加胎儿血红蛋白的生成。
鲍尔认为继续采用这种方法很重要。他说,“这些疾病是非常常见的遗传疾病,尤其是在世界上资源非常有限的地区。因此,我们需要广泛的治疗选择,以便为尽可能多的患者提供治疗。”
波士顿儿童医院是生物技术公司蓝鸟生物的股权持有人,一些作者已经申请了与治疗性基因编辑相关的专利。
如果这项正在研究中的技术被证明是有益的,那么波士顿儿童医院可能会获得经济效益。与所有研究一样,波士顿儿童医院已经采取并将继续采取一切必要措施来确保研究对象的安全,以及本研究中获得的信息的有效性和完整性。
参考资料:
人类造血干细胞高效治疗性基因编辑。自然医学,2019,doi:10.1038/s41591-019-0401-y。
本文来自生物谷。更多信息,请下载生物谷APP()