原文:汉克
全球罕见病药物市场依然火爆,越来越多的孤儿药进入临床II期和III期R&D阶段。很多国家的市场已经成熟,每年获批的孤儿药数量也大幅增加。我国也相继出台了减税、加快审批、将孤儿药纳入医保等措施。提高国内药企的R&D力,从而保障罕见病患者的用药权益。
一、罕见病及其用药基本含义
罕见病是一类发病率极低的疾病的统称,也称为“孤儿病”,治疗罕见病的药物也称为孤儿药。根据世界卫生组织的定义,占总人口0.65~1的疾病可以定义为罕见病。
根据国情,国际上罕见病的认定标准存在一定差异。比如美国把罕见病定义为患者少于20万的疾病;欧洲定义为2000年发病率小于1的疾病。我国对罕见病没有明确的定义,但一般认为成人患病率低于50万分之一、新生儿患病率低于1万分之一的疾病可以定义为罕见病。基于上述定义和估算,美国已有7000多种疾病被定义为罕见病,其中只有约400种罕见病有相应的治疗药物获批。世界范围内,罕见病患者总数已达3亿,我国罕见病患者约2000万,每年新增患者20万以上。
二、全球罕见病领域产业发展现状及趋势研究
1. 全球罕见病用药市场持续快速增长
全球罕见病药物市场火热,已经成为新药研发的主战场。据悉,2018年,全球罕见病药物市场规模为1310亿美元,以12.3%的年复合增长率快速增长,预计2024年将达到2420亿美元。稀有药物市场的增长率是同期非稀有药物市场(6%)的两倍。预计到2024年,其在处方药市场的份额将首次超过20%。
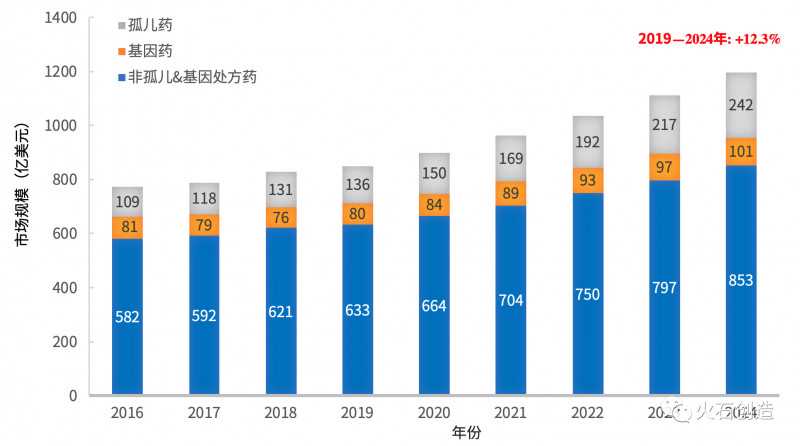
图12016—2024全球罕见病药物市场格局(翻译错误,单位修正为10亿美元)
2. 多个国家市场成熟,孤儿药资格及获批数显著增长
在美国实施《孤儿药法案》之前(1983年之前),只有38种FDA批准的新药用于治疗罕见病。《孤儿药法案》通过后,从1983年到2018年,FDA批准了770种孤儿药,授予了约4860种资格。2014年至2018年,孤儿药获批数量较1998年前大幅增加。
2018年,FDA批准了59个新的分子实体,其中34个(58%)新药用于治疗罕见疾病。FDA批准的孤儿药中,70%用于治疗肿瘤疾病,其中270种为孤儿药,适应症与非霍奇金淋巴瘤(NHL)相关,其次为急性髓系白血病220种,胰腺癌189种。2018年,FDA批准用于治疗霍奇金淋巴瘤、急性髓细胞白血病和胰腺癌的孤儿药数量仍然最多,说明目前肿瘤疾病仍缺乏有效的医疗手段。
表1已批准的孤儿药在孤儿药认证中的比例
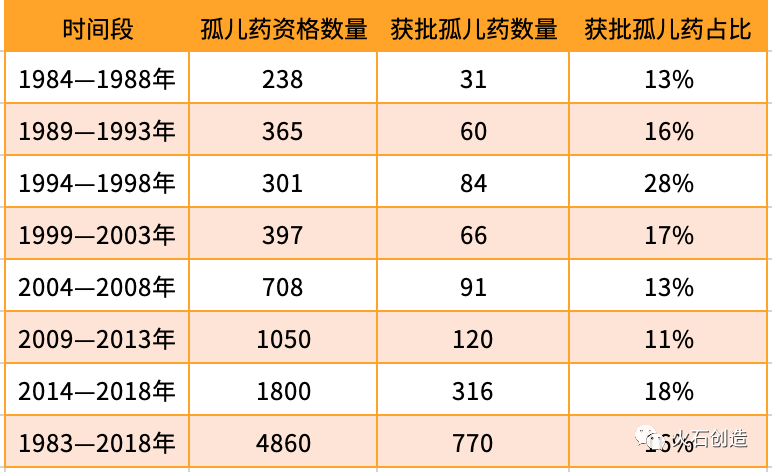
3. 罕见病用药研发投入逐见成效,迎来成果收获期
根据塔夫茨CSDD(塔夫茨大学药物R&D研究中心)的数据,2015年有766项针对罕见病的药物临床试验,2018年增加到942项,年增长率为8.9%。约84%的罕见病药物新临床试验处于I期和II期开发阶段。稀有药物II期和III期临床试验的增长率超过12%,是I期临床试验增长率的两倍以上,这表明稀有药物的R&D投资正在逐一取得成效。
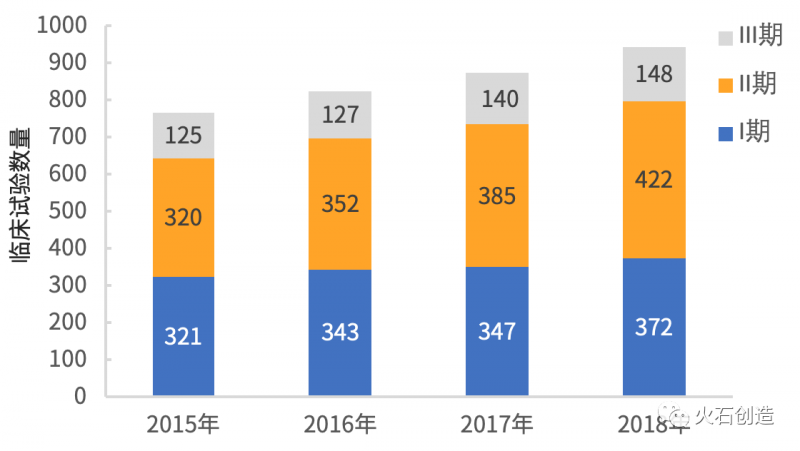
图2 2015-2018年罕见病药物临床试验数量
三、国内罕见病领域产业发展现状及趋势研究
1. 国内罕见病用药行业处于早期阶段,2018年后多政策助力发展提速
长期以来,我国没有罕见病的统计数据和目录,也没有明确的罕见病用药定义,因此罕见病领域的药品注册和生产没有快速发展。2018年以来,我国陆续出台相关政策,支持罕见病药物研发。
2018年5月,官方首次颁布《第一批罕见病目录》,统计121种疾病,加强国家对罕见病的管理。
2019年2月,国务院对首批21个罕见病药品和4个原料药实施降税。我
目前,国内已经诞生了北海康成、英诺医药、北京科信毕成等罕见病研发企业。其中,北海康成建立了国内首个罕见病药物研发和商业整合平台,通过引进国外技术和自主创新,推动罕见病药物在国内上市。
表2罕见病降税药品清单
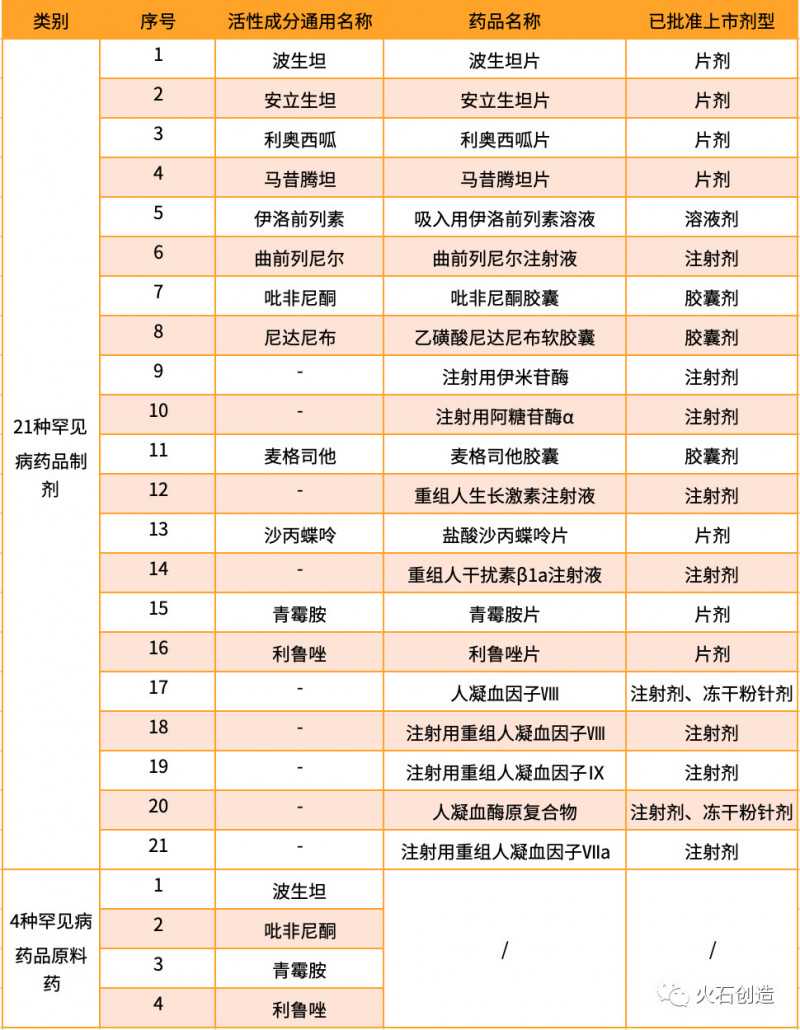
2. 罕见病用药国内支付模式仍在探索阶段,市场形成需时间考验
稀有药物的性质决定了它的高价。在世界范围内,许多国家都建立了完善的罕见病药品支付体系,商业保险极大地缓解了罕见病患者的经济压力。而在我国,罕见病的医疗费用大多由患者自己承担,而罕见病患者大多不能正常工作,因病致贫的情况很多,可支配资金非常有限。因此,我国罕见病的配套支付机制仍需探索。
根据《2019中国罕见病药物可及性报告》,目前我国上市的具有罕见病适应症的药品有55种,其中纳入医保的罕见病药品只有29种,涉及18种罕见病。9种罕见病药品按国家医保目录甲类报销,用于治疗11种罕见病适应症。病人在使用它们的时候不需要付费。目前更多的罕见病药物出现在医保谈判目录中,未来完善的支付体系将极大激活国内罕见病药物市场,让更多国内药企愿意投入罕见病药物研发,患者有药可用。
四、小结
目前,全球罕见病药物研发的热度持续不减,越来越多的孤儿药正在进入临床研发的二期和三期,并逐步投放市场。每年获批的孤儿药数量也大幅增加。这有望改变很多罕见病患者很少或没有药物可供选择的窘境。
近年来,我国政府通过出台减税、加快审批、将孤儿药纳入医保等相关措施,提高国内药企的R&D力,保障罕见病患者的权益。我们有理由相信,我们国家的步伐会越来越快,越来越多的罕见病会被攻克,越来越多的罕见病患者能得到病有所医,药有所保。