杜氏肌营养不良症(DMD)是一种X连锁的隐形遗传病,大约每5000名男性中就有一人患病。尽管近年来基于细胞和基于基因的治疗取得了进展,但DMD仍然是一种毁灭性的疾病,治疗方法非常有限。该疾病的主要原因是肌营养不良蛋白的丢失,该蛋白通过连接肌细胞内部的细胞骨架和细胞外基质来提供肌纤维膜的机械稳定性。此外,巨噬细胞是DMD肌肉中最丰富的白细胞,其异常持续和异常产生的炎症介质在促进疾病进展中起着关键作用。
在前期研究中,研究人员构建了缺乏趋化因子受体CCR2的营养不良小鼠(mdx小鼠,DMD模型),证明了骨髓(单核细胞)源性巨噬细胞(BMDM)在疾病早期发病中的重要性。发现在mdx小鼠中Toll样受体4 (TLR4)的基因切除可以产生有益的效果,并使肌内巨噬细胞更加抗炎。然而,这些现象背后的细胞机制尚未完全了解。

研究人员研究了营养不良的mdx小鼠和年龄匹配的野生型(WT)对照组在基本条件下培养7天后BMDM的变化。发现骨骼肌坏死前mdx的BMDM中许多促炎基因和抗炎基因明显上调,且大部分在纤维化后期仍呈低程度上调。这表明在骨骼肌营养不良的病理发生过程中,骨髓中产生巨噬细胞的前体细胞的功能发生了变化。此外,还分析了mdx BMDM在不同疾病阶段的代谢变化。在坏死期,与同龄WT组相比,mdx BMDM组小鼠的基础耗氧率和最大耗氧率显著降低。在老年小鼠中,mdx组乳酸浓度在坏死期升高,在纤维化期降低。
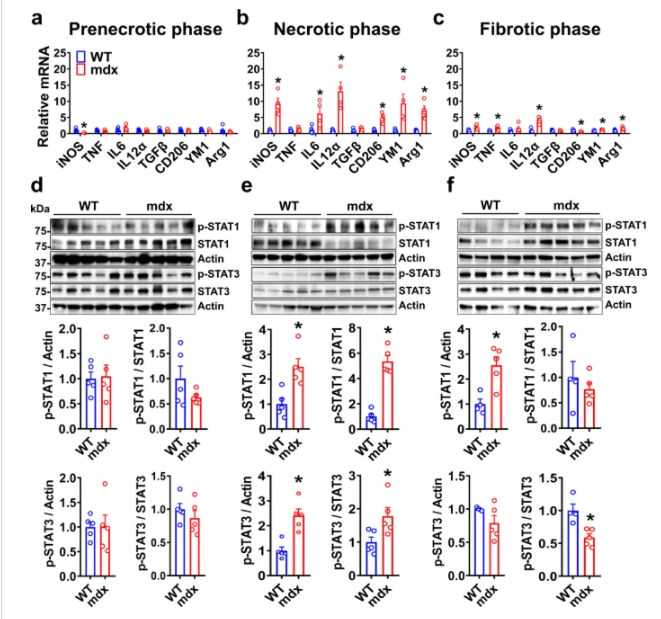
mdx BMDM基础炎症状态下疾病发展阶段的变化
为了确定mdx BMDM在暴露于外来刺激后是否表现出非特异性基因转录反应的扩增,研究人员进行了各种不相关的次级刺激(细胞因子,PAMPs/DAMPs)。数据显示,mdx小鼠慢性全身性骨骼肌坏死后,BMDM发生了巨大变化,对各种不相关的炎症刺激表现出显著的高反应性。此外,在mdx小鼠BMDM中,肌肉损伤相关分子如粉碎的骨骼肌提取物和纤维蛋白原可用作训练免疫诱导的主要“训练刺激物”。
进一步的研究发现,在mdx BMDM中观察到的对无关的继发性炎症刺激的高反应性和代谢表型的改变在很大程度上被TLR4缺陷消除,这表明肌营养不良小鼠中异常BMDM的表观遗传和功能特征是TLR4依赖性的。此外,小鼠BMDM的表型变化显示了训练免疫的标志性特征,包括骨髓移植到非营养不良小鼠后免疫的遗传性和持久性。因此,训练免疫可能是DMD病理性炎症的重要机制。(生物谷)
参考文献:巴特拉伊,s,李,q,丁,j等TL是杜氏肌营养不良鼠模型中训练免疫的调节剂。全国社区13,879 (2022)。https://10.1038/S41467-022
本文来自生物谷。更多信息,请下载生物谷APP()