日前,国务院下发关于落实《关于规范医疗机构开展新型冠状病毒肺炎药物治疗临床研究的通知》的函(以下简称通报函)回应新冠肺炎疫情联防联控机制科研组,进一步细化了新冠肺炎肺炎药物临床研究。
《通知函》规定临床研究实行医疗机构审批制度,医疗机构应当与临床研究负责人签订临床研究项目任务书,并在3日内向颁发其医疗机构执业许可证的卫生行政部门备案临床研究,在医学研究登记备案信息系统中上传相关信息。对于已经开展(第一受试者已入组)但尚未完成的临床研究,医疗机构应当在本文发布之日起3个工作日内完成。逾期未完成的医疗机构不得继续开展临床研究工作。
对于临床研究的开展流程,《通知函》要求省级卫生行政部门每天通过备案系统收集辖区内医疗机构拟开展临床研究的相关信息,转发同级科技行政部门并报送联防联控机制研究组长科技部办公厅。然后由课题组下设的药物研发专班(中国生物技术发展中心)组织专家进行讨论,提出是否推荐临床研究的书面意见。对推荐临床研究的品种,课题组办公室将推荐意见转国家卫生健康委科教司,国家卫生健康委科教司会同医政医管局协调医疗机构承担临床研究任务。
省级卫生行政部门跟踪临床研究进展,汇总临床研究成果,转发同级科技行政部门,由科技行政部门报送科技部。研究小组将统一收集相关研究信息,经专家审核后,将效果较好的药物信息(包括建议用法用量、禁忌症及可能的毒副作用等。)将上报联防联控机制医疗救治组。
值得一提的是,《通知函》还建议医疗救治组组织专家研究,提出相关药物是否纳入诊疗方案进一步试验的意见。未纳入诊疗计划的旧药,不得大规模直接用于临床。
2月25日,国家卫健委、科技部、国家美国食品药品监督管理局发布《关于规范医疗机构开展新型冠状病毒肺炎药物治疗临床研究的通知》,对上市药物临床研究进行了协调和规范,进一步明确了开展研究的条件。《通知》提出临床研究的药物应为上市药物,经体外实验和动物实验验证,研究机构应为新冠肺炎县级以上治疗指定医院,包括收容所医院。研究负责人应是具有大专以上学历的执业医师,能够针对可能存在的风险制定计划和管理措施。医疗机构是负责临床研究的主体。
自新型冠状病毒疫情爆发以来,新冠肺炎全国各地掀起了治疗药物临床试验的热潮。据益谷边肖通过中国临床试验注册中心官网查询,截至4月9日02: 01,新冠肺炎共有583项临床试验,涉及连花清瘟、血必净、洛匹那韦/利托那韦、阿比朵尔、磷酸氯喹、糖皮质激素、热毒宁注射液、子宫血干细胞等药物。
根据临床试验数据库收集的数据,最早的新型冠状病毒临床研究于1月23日注册,是由武汉金银潭医院(武汉于
此前,北京、上海、广州、南京、Xi安等地科研机构的多位卫生统计和流行病学专家发表了《关于科学、规范、有序地开展新型冠状病毒肺炎相关临床试验的建议》篇文章,对新冠肺炎目前的肺炎临床试验提出了批评和建议。
上述专家指出,如果没有高质量的临床试验设计,如样本量不足、对照组选择不合理、分组随机化和掩蔽执行不严、疗效指标评价标准不客观、数据完整性和真实性保障不足等,那么这些临床研究将难以提供高质量的有效性和安全性证据,使首次试验患者、研究者和管理部门的努力付诸东流。
也有业内人士指出,现在很多临床试验都是小样本,很多都不是随机对照、双盲的。很难产生有意义的结果,有些甚至有挤占资源的嫌疑,导致一些很有前途的药物临床试验招不到病人的尴尬。
因此,本次《通知函》提出,如有违反《通知》、《传染病防治法》、《药品管理法》、《药物临床试验质量管理规范》、《干细胞临床研究管理办法》等相关规定和要求,且有明显毒副作用或无。
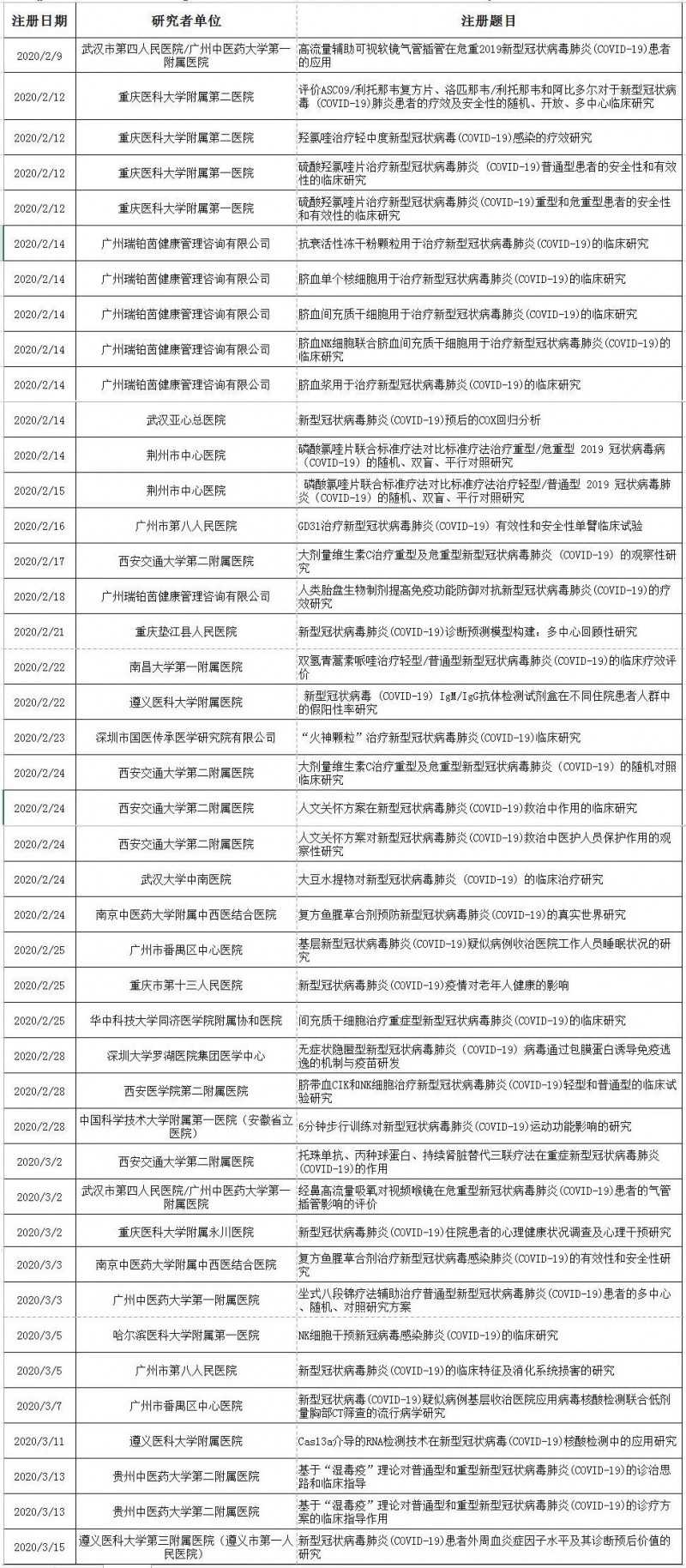
在上述583项注册临床试验中,有43项临床研究被取消,包括《6分钟步行训练对新型冠状病毒运动功能影响的研究》(新冠肺炎)、《坐位八段锦疗法治疗常见新型冠状病毒的多中心随机对照研究方案》(新冠肺炎),以及脐带血间充质干细胞、脐带血CIK和NK细胞、脐带血NK细胞联合脐带血间充质干细胞。
原标题:新冠肺炎药物临床实践被国务院整顿:取消43项研究,包括坐八段锦和6分钟步行训练。