2006年12月2日,是一个注定被载入医药工业史册的日子。这一天,辉瑞宣布其降胆固醇药物torcetrapib的三期临床试验失败,该试验有超过15,000名参与者。虽然辉瑞公司在torcetrapib的研发上投入了超过8亿美元,但它不得不停止开发这一新药项目。
Torcetrapib临床试验失败的消息在心血管疾病研究领域乃至整个医药行业引起强烈震动。每个人都很好奇开发CETP抑制剂的其他制药公司会有什么反应。诚然,一些制药公司立即停止了CETP项目,但默克、罗氏、礼来公司和安进并没有选择放弃。至于原因,还得从CETP抑制剂的作用机制和早期的研发过程说起。
I
HDL假说
脂类物质,包括脂肪和胆固醇,是维持人体正常功能所必需的。但由于脂肪、胆固醇等脂质是疏水性物质,必须与载脂蛋白等其他物质结合形成脂蛋白,才能在血液中运输。根据脂蛋白的大小和密度可分为乳糜微粒、极低密度脂蛋白(VLDL)、低密度脂蛋白(LDL)和高密度脂蛋白(HDL)。每种脂蛋白都有特定的功能。
回肠吸收的胆固醇和甘油三酯被运输到淋巴,以乳糜微粒的形式进入血液。甘油三酯被脂蛋白脂肪酶水解后被肌肉和脂肪组织吸收形成甘油和脂肪酸,而含有胆固醇酯的乳糜微粒残基可进入肝脏,与肝细胞上的特异性受体结合后通过胞吞作用进入肝细胞。胆固醇可以在肝脏中被氧化,并作为胆汁排泄到胆固醇运输的内源性途径中。
在内源性途径中,胆固醇和新形成的甘油三酯以VLDL的形式运输到肌肉和脂肪组织,甘油三酯以甘油和脂肪酸的形式被这些组织水解和吸收。在这个过程中,VLDL中的甘油三酯减少,体积逐渐变小,但胆固醇酯不能被吸收。最后,VLDL会形成含有大量胆固醇酯的脂蛋白LDL。但是,LDL的功能与VLDL明显不同。细胞可以通过识别apoB-100的LDL受体介导的内吞作用吸收LDL,从而获得类固醇合成和嵌入细胞膜所需的胆固醇。但是LDL在动脉粥样硬化的病理过程中也起着重要的作用。
LDL可以侵入动脉内膜,逐渐被氧化。氧化的低密度脂蛋白可损伤内皮细胞并引起炎症反应,炎症反应可使内皮细胞表达VCAM-1并从血液中募集单核细胞进入动脉内膜。单核细胞分化为巨噬细胞后,可以吞噬氧化型LDL,逐渐形成泡沫细胞,细胞内含有大量脂质。泡沫细胞会逐渐死亡,释放氧化脂质,进一步诱发炎症反应。同时,泡沫细胞可诱导平滑肌细胞向内膜迁移和增殖,促进胶原形成,导致动脉内膜斑块硬化。
在几十年的斑块形成过程中,患者不会有明显的症状,但随着斑块的逐渐增大和硬化,在斑块形成的部位可能会发生血管破裂。一旦形成血管破裂,会立即引起血液凝固,堵塞血管。血管完全闭塞可导致心肌缺血损伤,也称心肌梗死。虽然低密度脂蛋白不是诱发动脉粥样硬化的唯一因素,但从上述过程中可以清楚地了解低密度脂蛋白在病理过程中的重要性,这也是LDL-C被称为坏胆固醇的原因。
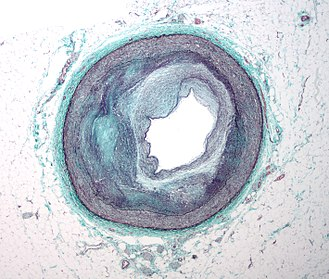
动脉粥样硬化
还有另一种生理机制称为体内胆固醇逆向转运(RCT),可以将胆固醇从泡沫细胞转移到肝脏。高密度脂蛋白是介导这一过程的重要成分,我们通常称HDL-C为好胆固醇。基于上述现象,研究人员还提出了HDL假说:血液中HDL浓度的降低阻碍了动脉内膜对胆固醇的清除,加速了动脉粥样硬化的形成,从而导致缺血性心脏病。关于HDL假说有两个潜在的重要论点:一个是RCT过程部分依赖于HDL功能,另一个是低HDL水平的人比高HDL水平的人患心血管疾病的风险更高。
那么如何根据HDL假说研发药物呢?虽然理论上所有明显影响RCT过程的分子都可能成为药物研发的目标,但RCT是一个非常复杂的过程。起初,研究人员很难确定影响这一过程的关键分子。
最终,研究人员瞄准了CETP(胆固醇酯转移蛋白)。CETP主要由肝脏分泌。进入循环系统后,可与HDL颗粒结合,可介导胆固醇酯从HDL向LDL和VLDL转移,从而影响不同脂蛋白中的胆固醇含量。研究人员关注CETP的原因是基于一项流行病学研究。1990年11月《新英格兰医学杂志》发表了一篇论文[1],报道了一个日本家庭由于基因缺陷导致CETP蛋白功能缺陷,导致体内HDL水平升高,没有证据表明有该基因缺陷的家庭成员会过早患动脉粥样硬化。
虽然有证据证明CETP水平与HDL之间的相关性,但不同实验得出的结论并不一致[2]。例如,流行病学研究发现,尽管一些人没有CETP,但他们仍可能患有心血管疾病。研究人员还在老鼠和兔子动物模型中研究了CETP的活性。小鼠模型的结果不一致,很难得出令人信服的结论。然而,对兔子的研究发现,抑制CETP可以提高HDL水平,降低动脉粥样硬化的发生率。但从理论上讲,也有人担心抑制CETP会导致体内体积巨大、功能异常的HDL/LDL堆积。尽管如此,几家制药公司很快开始了CETP抑制剂的研发。毕竟,只有通过临床试验,我们才能验证抑制CETP是否能影响心血管事件的发生率。
制药公司对CETP抑制剂的热情不仅仅是基于这些早期的流行病学研究和动物模型实验数据。虽然当时市场上有几种他汀类药物,但它们只能降低25%左右的主要心血管事件风险。心血管疾病仍然是全球范围内的主要死亡原因,大约五分之一使用他汀类药物的人会出现药物相关的副作用。因此,进一步降低心血管疾病的风险,寻找替代药物成为制药公司关注的焦点。
患者的胆固醇相关问题并不仅限于高LDL水平,部分患者还存在低HDL水平和高甘油三酯水平。因此,寻找能与他汀类药物产生协同作用,降低甘油三酯水平,提高HDL水平的药物是当时药物研发的重要方向。
II
折戟
文章055-79000发表后不久,辉瑞开始了CETP的研究项目。然而,研究人员发现,CETP抑制剂的分子设计和优化极其困难。CETP是一种高度亲脂的蛋白质,所筛选的抑制剂不仅活性弱,而且水溶性极差。在该项目开始后的几年内,药物化学家筛选了数十万种小分子,但仍未能找到具有所需特性的化合物,该项目数次暂停。
辉瑞公司的项目主管请一位名叫罗杰鲁格的年轻人接手,作为最后的尝试。鲁格很快发现了一种能与CETP发生微弱相互作用的小分子,经过不断的结构优化,其活性提高了100倍。虽然这种小分子的溶解性还很差,但在制剂专家的帮助下,他们终于完成了临床前的研究。完成这项临床前研究的小分子化合物是torcetrapib。
1999年,torcetrapib进入I期临床研究。研究人员发现,torcetrapib不仅以剂量依赖的方式显著增加HDL-C水平,还显著降低LDL-C水平,这显然大大超出了研究人员的预期。辉瑞公司对这些临床试验的结果感到非常兴奋。而且torcetrapib的安全性没有明显问题,但是研究人员发现,在高剂量的情况下,患者的血压会升高。
辉瑞的临床研究也吸引了其他制药公司的注意。同期,罗氏收购了日本烟草的dalcetrapib,默克和礼来也加快了CETP项目的研发。然而,torcetrapib在II期临床试验中出现了奇怪的现象。研究人员发现,torcetrapib对不同患者的LDL水平有不同的影响。一些患者的LDL水平下降,而另一些患者的LDL水平明显上升。然而,他们发现,在他汀类药物组合后,这种差异会消失。因此,在III期ILLUMINATE研究中,研究人员选择torcetrapib联合立普妥来评估该方案与立普妥之间心血管事件的差异。
ILLUMINATE单次临床试验预算近8亿美元,这可能是当时整个制药行业最昂贵的临床试验。虽然早期临床数据显示torcetrapib可以增加HDL水平,阿托伐他汀可以降低LDL水平,但HDL/LDL水平的变化是否可以转化为心血管益处仍是未知的。
2006年12月2日,辉瑞公布了ILLUMINATE临床试验结果:torcetrapib/阿托伐他汀联合组死亡人数明显高于对照组(82 vs 51),临床试验失败。辉瑞还宣布在同一时期停止torcetrapib的临床开发。辉瑞公司的CETP项目已经走过了15个年头,但它仍然没有获胜。

III
锲而不舍
在torcetrapib的早期临床研究中,辉瑞的研究人员发现该药物可能导致血压升高。然而,由于血压升高的程度不是很大,辉瑞员工和外部专家一致认为,torcetrapib增加HDL的健康益处可以抵消血压升高的影响,因此在没有进一步研究的情况下开始了III期临床研究。
辉瑞显然低估了这种副作用的影响。现在回想起来,辉瑞当时比较明智的选择是放弃torcetrapib,选择其他没有高血压副作用的CETP抑制剂重启临床研究,但当时的辉瑞显然不同意这种策略。促进快速CETP抑制剂torcetrapib的临床研究显然不仅仅是基于未满足的临床需求。考虑到立普妥的专利到期,辉瑞当时的管理层压力很大。所以某种程度上,全力推进torcetrapib的临床研究也是无奈之举。从科学的角度来看,放弃torcetrapib,选择其他候选药是更合理的选择,但这也意味着药物的潜在上市时间必须推迟数年,辉瑞等不起。
torcetrapib临床试验失败后,ILLUMINATE项目的研究人员开始分析临床试验失败的原因。通过分析患者的血液指标,他们发现了与死亡风险增加相关的几个因素:患者血钾水平降低、血钠和碳酸盐水平升高以及醛固酮水平升高[3]。因此,研究人员推测torcetrapib临床试验的失败是由脱靶效应引起的。
与此同时,其他正在研发CETP抑制剂的制药公司也在积极寻找torcetrapib失败的原因,并开始反复验证自己的CETP抑制剂的安全性。
当辉瑞宣布torcetrapib的临床试验失败时,没有人确定是CETP靶点本身还是药物分子缺陷导致了试验失败。因此,默克推迟了自己的CETP抑制剂anacetrapib的开发,专注于这种药物的毒性。在临床前动物模型研究中,默沙东发现虽然torcetrapib可以引起血压和醛固酮水平的升高,但他们自己的anacetrapib并没有产生这样的作用[4],临床研究中也没有发现anacetrapib引起醛固酮水平和血压升高的现象。因此,他们推测血压升高只是由torcetrapib自身缺陷导致的脱靶效应引起的。

默沙东进一步研究了CETP抑制剂和HDL的详细作用机制,比较了anacetrapib、torcetrapib和罗氏的dalcetrapib对CETP和HDL功能的不同影响[5]。还发现服用anacetrapib的患者可以提高HDL的保护作用[6]。所以默克小心翼翼地推进临床研究。
起初,他们只是进行了一项只有1600名患者的中等规模临床试验,代号为DEFINE。DEFINE研究发现,anacetrapib不会像torcetrapib一样增加心血管疾病的风险,经过分析发现,服用anacetrapib的患者LDL水平可降低39.8%,HDL水平可升高138.1%。因此,默克公司开始了另一项针对3万多名患者的REVEAL临床研究,以确定抑制CETP是否可以降低心血管事件的风险。
当辉瑞宣布torcetrapib临床试验失败时,礼来公司的evacetrapib仍处于临床前研究阶段。早在2004年,当辉瑞报告torcetrapib可能会升高血压时,礼来公司就开始筛选不会引起高血压的CETP抑制剂。然而,在辉瑞公司报道torcetrapib可导致电解质失衡并增加醛固酮水平[3]后,他们也开始了体外实验,以验证evacetrapib是否具有相同的性质[7]。
Evacetrapib的I期临床研究也很仔细。礼来公司对该药的性质做了详细的研究,但没有发现该药能产生明显的副作用,也没有出现血压升高、电解质紊乱等现象。期临床试验结果显示,evacetrapib可使HDL水平升高129%,LDL水平降低36% [8]。
torcetrapib的临床试验失败后,罗氏开始更详细地研究dalcetrapib的安全性。罗氏进行了大规模的III期临床试验(dal-OUTCOMES),共有15600名患者,同时进行了两项IIb期临床研究(代号dal-VESSEL和dal-PLAQUE),研究药物的安全性[9]。两项安全性临床研究表明,dalcetrapib可使HDL水平升高31%,而不会引起高血压。Dal-PLAQUE使用血管造影术来研究dalcetrapib治疗对动脉导管的影响。服药两年后,他们没有发现任何患者的动脉壁异常[10]。
即使公司如此小心翼翼,也无法得到想要的结果。2012年,罗氏暂停临床研究,原因是达西妥昔布不能产生预期疗效。2015年10月,礼来宣布evacetrapib的三期临床试验未能加速。与安慰剂相比,evacetrapib不能降低心血管事件的发生率。
今年6月,默沙东公布了anacetrapib的III期临床试验结果REVEAL:与安慰剂/阿托伐他汀相比,anacetrapib/阿托伐他汀的心血管事件发生率分别为10.8%和11.8%。虽然已经达到了主要终点,但很明显,仅降低9%的心血管事件风险无法与疗效更明确的PCSK-9抑制剂竞争。今年10月,默沙东宣布放弃anacetrapib的上市申请。受默沙东anacetrapib的影响,安进立即宣布放弃研发自己的CETP抑制剂obicetrapib。
IV
逻辑线
我们来看看CETP抑制剂作用机制的逻辑:CETP抑制剂抑制CETP蛋白的功能,提高HDL-C水平,影响HDL功能,影响RCT进程,影响心血管疾病(CVD)的发病率。到底出了什么问题?
默沙东、罗氏和礼来都认为辉瑞的CETP抑制剂失败可能是由于托塞曲匹药物分子的缺陷导致脱靶效应,导致血压升高、电解质失衡、醛固酮水平异常等问题。对于很多小分子药物靶点来说,前期合理的化合物设计和结构优化,确实有可能提高小分子的选择性,减少脱靶效应。Anacetrapib、dalcetrapib和evacetrapib没有torcetrapib高血压的缺陷。在抑制CETP蛋白的功能链接方面不太可能存在问题。
那么抑制CETP会增加HDL-C水平吗?让我们来看看礼来公司埃瓦西特拉皮的数据。高密度脂蛋白增加125%,低密度脂蛋白减少30% [11],那为什么还需要自行车呢?但问题是,提高HDL-C水平呢?evacetrapib对心血管事件的发生率没有影响。
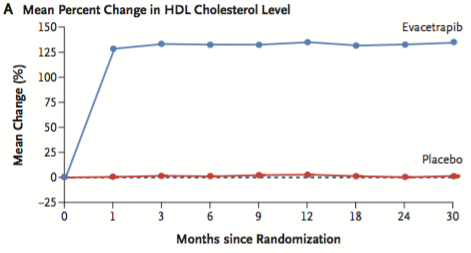
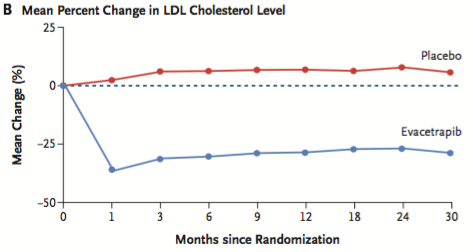
关键问题是HDL-C和心血管疾病之间的关系是什么?
首先需要说明的是,HDL假说是基于HDL的保护作用,而不是HDL-C,所以应该在临床试验中验证的是HDL的保护作用,而不是HDL-C。影响高密度脂蛋白功能的因素不仅仅限于HDL-C水平,还包括高密度脂蛋白颗粒数、前-高密度脂蛋白水平和其他高密度脂蛋白成分。但由于HDL水平难以检测,临床试验中一直采用HDL-C作为检测指标。影响HDL-C水平的因素很多,但并不是所有HDL-C水平的变化都与RCT过程有关。
接下来,最关键的问题是HDL的功能与CVD有什么关系。换句话说,HDL假说是真的吗?可惜还是没有定论。高密度脂蛋白可能确实具有保护作用,而RCT可能确实减缓了动脉粥样硬化的疾病进程。但由于HDL成分复杂,无法确定哪种类型的HDL有保护作用或哪种类型的HDL受CETP抑制剂的影响,导致了anacetrapib对CVD保护作用弱,torcetrapib增加患者死亡率,而evacetrapib无CVD保护作用的明显差异。
但anacetrapib的CVD保护作用也可能是由于LDL生成减少,HDL和CVD可能只有相关性而没有因果关系,这就意味着HDL假说是错误的。但这只是猜测。HDL假说还有很多研究和验证性实验,希望未来能得到满意的答案。
之前看过作者写的阿尔茨海默病文章的读者,应该对HDL假说比较熟悉。HDL假说与淀粉蛋白假说有很多相似之处,基于淀粉蛋白假说的CETP抑制剂和BACE抑制剂的发展过程也有很多相似之处。对于药物化学家来说,基于BACE和CETP开发药物非常困难,但最终药物化学家成功获得了活性高、理化性质可接受的化合物。然而,由于我们对心血管疾病和阿尔茨海默病的知识缺乏,这些化合物都没有成功通过临床试验。
可能会有一部分学生或研究人员是新进入我国新药研发领域的,他们可能对新药研发领域有一种错觉,认为做新药无非就是换个剂型或者让我也或者我也担心。刚进实验室的时候,有一天老板突发奇想,提出要做CETP抑制剂,把这个话题交给了同时进实验室的同学王兴,告诉她先合成anacetrapib修炼者,再做结构改造。王花了很长时间合成anacetrapib,但是因为老板没有联系到合适的研究组做活性筛选,课题不了了之。
有时候我很羡慕为基因泰克或默克这样的制药巨头工作的制药化学家。他们是新药研发领域的世界顶尖科学家。他们拥有别人无法比拟的资源,他们的项目难度令人望而生畏。而且我一直很偏执,这些公司里有这么一群人。驱动他们工作的不是所谓的业绩,不是他们股票的涨跌,而是对科研最纯粹的热情,对未知的好奇,对治病救人的责任感。
——纪念我敬爱的祖母。
参考资料:
1.新英格兰医学杂志。323:1234-1238.1990.
2.动脉硬化、血栓形成和血管生物学。37(11)1-9.2003.
3.新英格兰医学杂志。357:2109-2122.2007.
4.英国药理学杂志。154(7):1465-73.2008.
5.脂质研究杂志,51:2739-2752。2010.
6.动脉硬化、血栓形成和血管:1430-1438。2010.
7.脂质研究杂志,52:2169-2176。2011.
8.(19):2099-2109.2011.
9.当前医学研究和观点。27:463-480.2007.
10.柳叶刀。378:15471559.2011.
11.新英格兰医学杂志。376:1933-1942.2017.
