01
研究背景
三阴性乳腺癌对标准化疗的耐药性与MAPK通路的上调有关。Cortini是一种MAPK/细胞外信号调节激酶(MEK)抑制剂,可增加对紫杉烷和程序性死亡配体1抑制剂的敏感性。COLET是一项三队列、II期研究,旨在评估局部晚期或mTNBC患者的一线cobitinib联合化疗(使用或不使用atilizumab)。
02
研究方法
COLET是一项随机、多中心、三队列II期研究(45个中心;12个国家),在雌激素受体阴性、孕激素受体阴性和HER2阴性的mTNBC患者或不能进行根治性切除术的局部晚期TNBC患者中,我们评估了康贝替尼或安慰剂与紫杉醇的组合(队列I)、康贝替尼与阿替利珠单抗和紫杉醇的组合(队列II)以及康贝替尼与阿替利珠单抗和nab-紫杉醇的组合(队列III)。
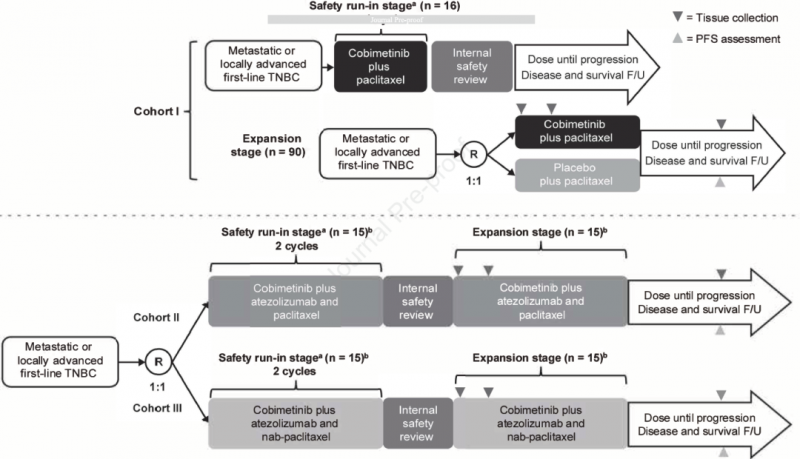
在安全导入期后,队列I中的患者(n=106)被随机分配接受1:1比例的康贝替尼(60 mg,在每个28天周期中D3-D23)或安慰剂联合紫杉醇(80 mg/m2,D1,8和15)。其他患者随机(1:1)进入队列II(n=32)或队列III(n=31),接受考比替尼联合阿替利珠单抗(840 mg,D1和D15)和紫杉醇或白蛋白结合紫杉醇(100 mg/m2,D1,D8和D15)。
主要终点是研究者评估的无进展生存期(PFS)(队列I)和确认的客观缓解率(ORR)(队列II/III)。此外,还评估了安全性/耐受性。
03
研究成果
在扩张阶段,群组I中的中位PFS在cobitinib/紫杉醇组中为5.5个月,在安慰剂/紫杉醇组中为3.8个月(风险比为0.73;95%可信区间:0.43-1.24;P=0.25)。
队列I的PFS曲线,考比替尼/紫杉醇组对比安慰剂/紫杉醇组(来源:Annal oncol)
在队列I中,康贝替尼/紫杉醇的ORR为38.3%(95%CI 24.40-52.20),安慰剂/紫杉醇的ORR为20.9% (95% CI 8.77-33.09)。队列II和队列III的ORR分别为34.4%(95%可信区间18.57-53.19)和29.0%(95%可信区间14.22-48.04)。
就安全性而言,所有队列中最常见的不良事件(AE)包括腹泻、恶心和皮疹。在队列I中,任何治疗组中2名患者最常见的3级AE包括腹泻、中性粒细胞减少和口腔炎;队列II或队列III中2名患者的3级AE为腹泻、贫血、中性粒细胞减少和中性粒细胞计数减少。
04
讨论
COLET是第一个评估PD-L1抑制剂、MEK抑制剂和紫杉烷(cobitinib和紫杉醇/白蛋白结合的紫杉醇)联合治疗局部晚期或mTNBC患者的研究。
此前,cobitinib已被批准与verMurphy联合用于晚期黑色素瘤患者,这些患者具有BRAF V600突变并对BRAF抑制剂单一疗法耐药,其中通过MEK激活MAPK是最常见的机制。鉴于MAPK途径的上调也可能导致mTNBC对紫杉烷耐药,研究人员假设—— cobitinib加紫杉醇可能导致中度临床改善。
然而,在队列I中,联合应用康贝替尼和紫杉醇并没有导致中位PFS或ORR的统计学显著增加,而是一种非显著的数值增加趋势。这可能与患者数量有限、统计设计、TNBC的异质性和其他导致紫杉烷耐药的潜在机制有关。
研究人员还假设—— cobitinib可能增加主要组织相容性复合体I和II、PD-L1的表达和分化簇8阳性T细胞的积累,从而使肿瘤对atilizumab敏感。
然而,在第二组和第三组中,阿替利珠单抗、cobitinib和紫杉烷的联合治疗仅显示中度临床缓解。与aissance 130相比,在nab-紫杉醇中加入atilizumab和安慰剂,ORR改善了约10%(56.0%对45.9%),显著延长了PFS (7.2对5.5个月)并增加了OS (21.0对18.7个月)。
考虑到COLET队列II/III中无病间期12个月的患者比例为23.8%,这种与预后不良相关的基线特征可能是导致上述明显差异的潜在因素。
此外,在COLET队列III中观察到的中位PFS(7个月)与assistance 130相似,尽管较短的中位随访时间限制了对OS获益趋势的解释。然而,队列II (3.8个月)中的低PFS可能是由于样本量小,与紫杉醇相比,nab-紫杉醇的治疗效果更好,以及早期复发患者的比例增加。

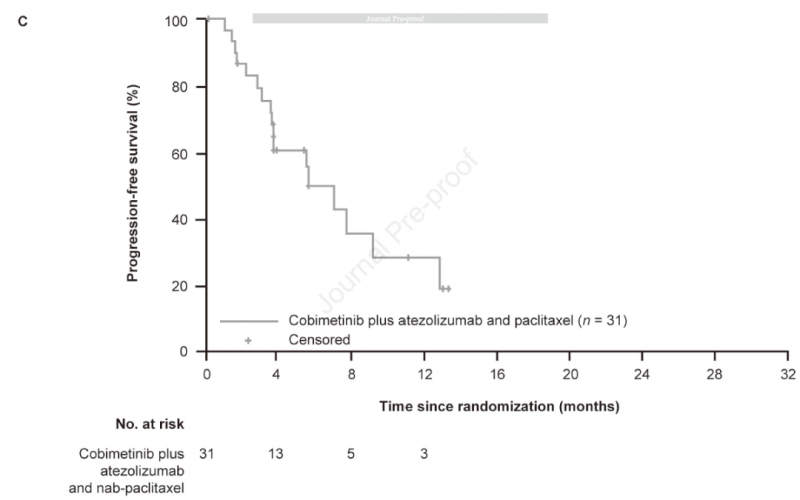
最后,值得注意的是,对COLET中组合生物标志物数据的回顾性和探索性分析显示,在——个队列II和III中,PD-L1阳性患者的ORR和PFS显示出改善趋势。这和《慷慨激昂》130是一致的。然而,缺乏对COLET中OS-PD-L1状态的相关性分析,队列II/III中的患者数量少,且没有安慰剂组,这意味着所有的比较都是描述性的,应仔细解释。
总之,在紫杉醇的基础上联合使用cobitinib并未导致PFS或ORR的显著统计学改善,但观察到数值增加的趋势并不显著。可替尼联合阿替利珠单抗和紫杉烷仅导致中度临床缓解,尤其是在PD-L1阳性人群中。
COLET研究初步证实了MEK抑制剂、化疗和免疫治疗在三阴性乳腺癌中的潜在活性。虽然没有计划进行进一步的试验来评估用cobitinib一线治疗mTNBC,但未来的研究将提高对TNBC其他MEK抑制剂治疗价值的理解。
技巧
基于全球首个联合BRAF和MEK抑制剂的免疫检查点抑制剂IMspire150的阳性III期临床试验,2020年7月,FDA批准阿替唑单抗联合cobimetinib和vemurafenib治疗BRAF V600突变阳性的晚期黑色素瘤患者。
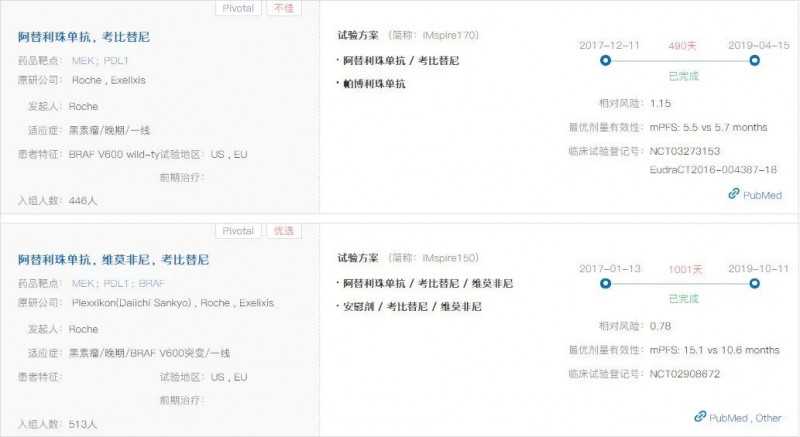
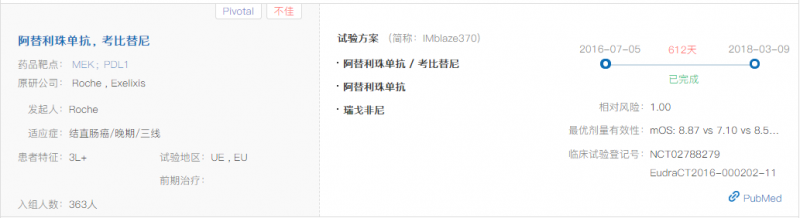
此外,阿替利珠单抗联合康贝替尼也被罗氏开发用于BRAF V600野生型黑色素瘤(IMspire170,不好)、晚期结直肠癌的后线治疗(IMblaze370,不好)、胆道癌(NCT03201458,阳性)、非小细胞肺癌的二线治疗(墨菲斯-PDAC,不好)和胰腺导管癌。
参考资料:
安Oncol。2021年2月1日;S0923-7534(21)00093-4。
doi: 10.1016/
