辉瑞(Pfizer)公司今日宣布,英国药品和健康产品管理局(MHRA)已批准口服JAK1抑制剂Cibinqo(abrocitinib)在英国上市,用于治疗适合接受全身性治疗的成人和12岁以上青少年中重度特应性皮炎(AD)患者。新闻稿指出,这是该疗法在全球范围内的首次获得监管机构的批准。
特应性皮炎是一种以皮肤炎症和皮肤屏障缺陷为特征的慢性皮肤病,其特征为红/紫斑、瘙痒、硬结/丘疹、渗液/结痂。它也是最常见的慢性复发性儿童皮肤病之一,在全球范围影响约10%的成人和约20%的儿童。许多中重度患者的病情控制不佳,需要额外的治疗方案来缓解症状。
Abrocitinib是一款口服JAK1抑制剂。JAK1抑制被认为可调节参与特应性皮炎病理生理学的多种细胞因子,包括白细胞介素IL-4、IL-13、IL-31、IL-22和胸腺基质淋巴细胞生成素(TSLP)。2020年10月28日,辉瑞宣布FDA接受了abrocitinib的新药申请,用于治疗12岁以上中重度特应性皮炎患者,并授予其优先审评资格。此前,该药还被FDA授予突破性疗法认定。
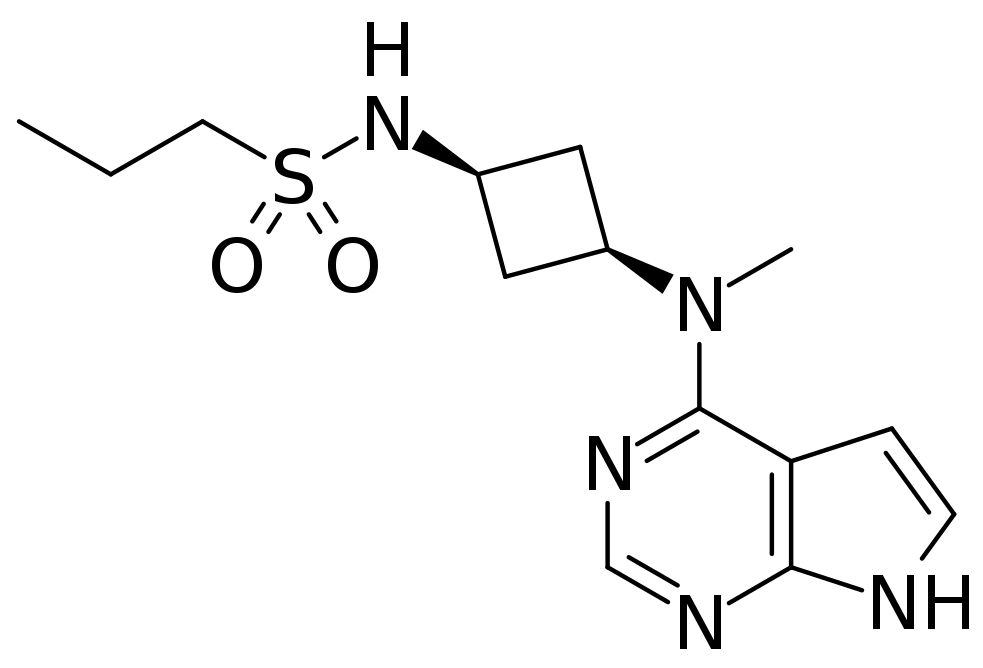
▲Abrocitinib分子结构式
Abrocitinib已经在多项3期临床试验中获得积极结果。例如,在名为JADE MONO-1的随机双盲,含安慰剂对照的3期临床研究中,接受治疗12周后,与安慰剂组相比,分别有43.8%和23.7%的患者皮肤症状达到或接近完全消失(IGA评分0/1),而在安慰剂组的数值为7.9%。而且,在治疗组中,分别有62.7%和39.7%的患者的湿疹面积和严重程度指数比基线改善至少75%(EASI 75),而安慰剂组中这一数值只有11.8%。
在名为JADE DARE的3期临床试验中,abrocitinib与获批抗体疗法相比,在每个评估的疗效指标上均具有统计学优效性。
目前,辉瑞已经向世界上多个国家和地区递交了abrocitinib的监管申请,包括美国、欧盟、澳大利亚和日本。
参考资料:
[1] UKs MHRA Grants Marketing Authorisation for Pfizers CIBINQO (abrocitinib) for Adults and Adolescents With Moderate to Severe Atopic Dermatitis. Retrieved September 9, 2021, from
(原文有删减)