5月31日,普利制药发布公告称,公司于近日收到FDA的注射用比伐卢定仿制药批准通知书。该产品是该公司生产的同类产品之一。据资料显示,该公司早前已获得七项产品的ANDA编号,这对该公司拓展美国市场有正面影响。
表1:普力药业获批产品信息
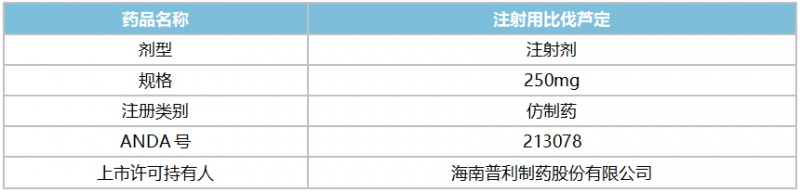
图1:国内市场已获得注射用比伐卢定生产批件的企业。
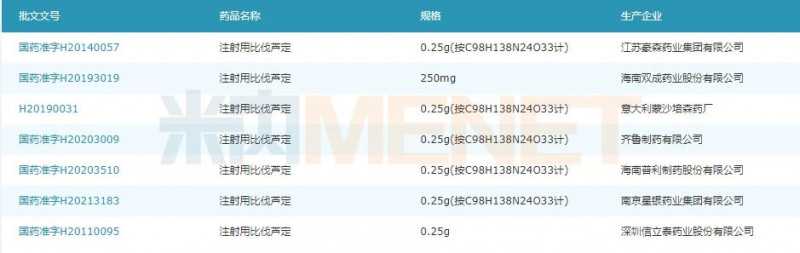
注射用比伐鲁丁是一种合成抗凝剂。2020年,其在中国城市公立医院、县级公立医院、城市社区中心、乡镇医院(简称中国公立医疗机构)的终端销售额超过5亿元。海南普利制药4种仿制药上市申请于2020年9月获批,视为通过评估。目前国内市场已有7家药企获得该产品的生产批文(包括1家原研和进口)。
普利制药在公告中提到,公司注射用比伐卢定属于共线生产品种,已于2020年12月获得FDA临时批准。目前美国的原产品仍在专利保护中,专利期限截止到2029年1月27日。
2021年1月,普利制药向FDA提交了PIV专利(申请的仿制药相关专利无效或仿制药不侵权)声明,同时也对原研究公司的上市许可持有人和专利持有人发起了专利挑战。在收到通知后45日内,原研究公司未对普利制药对注射用比伐卢定的专利挑战提起任何诉讼,即该公司的注射用比伐卢定ANDA挑战专利成功。随后,该公司向FDA通报了上述进展,并提交了注射用比伐卢定仿制药的最终上市审批申请。近日,公司收到FDA的上市批准通知,表明公司具备在美国销售注射用比伐卢定的资格。
表2:普利制药早前获得的ANDA数
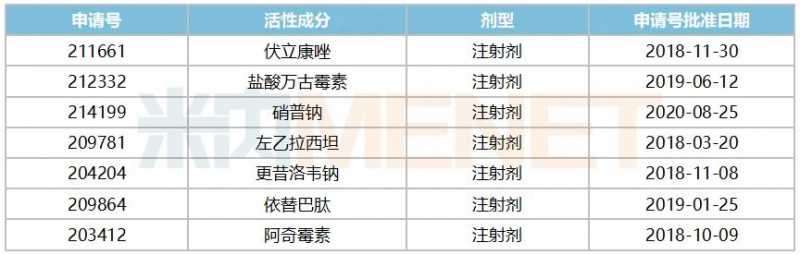
根据Minenet的数据,普力药业较早获得了7个产品的ANDA编号。此次注射用比伐卢定获批,将有助于提升公司在美国市场的销售业绩。