随着我国利好政策的不断释放和创新能力的不断提升,越来越多的创新药物已经进入或即将进入临床试验阶段。相比之下,临床研究资源处于紧张状态,包括临床试验机构数量少,现有临床试验机构承载能力和研究水平有限等。临床研究资源的供需矛盾日益成为制约我国新药创新的巨大瓶颈。未来,搭建临床资源服务平台将成为解决临床试验机构失衡、供需矛盾的重要抓手。
一、我国药物临床试验机构资格认定概况
据燧石族创建的数据库显示,自2005年实施《药物临床试验机构资格认定办法(试行)》以来,中国药物临床试验机构(GCP)获得了国家药品监管部门的认可。截至2019年8月底,共有583家药物临床试验机构,710份资质证书在有效期内。
但从历年来全国获得认证的临床试验机构数量来看,2005年至2016年,数量没有明显变化。自2017年以来,中国已获认可的临床试验机构数量大幅增加,达到2017年前的2倍左右。
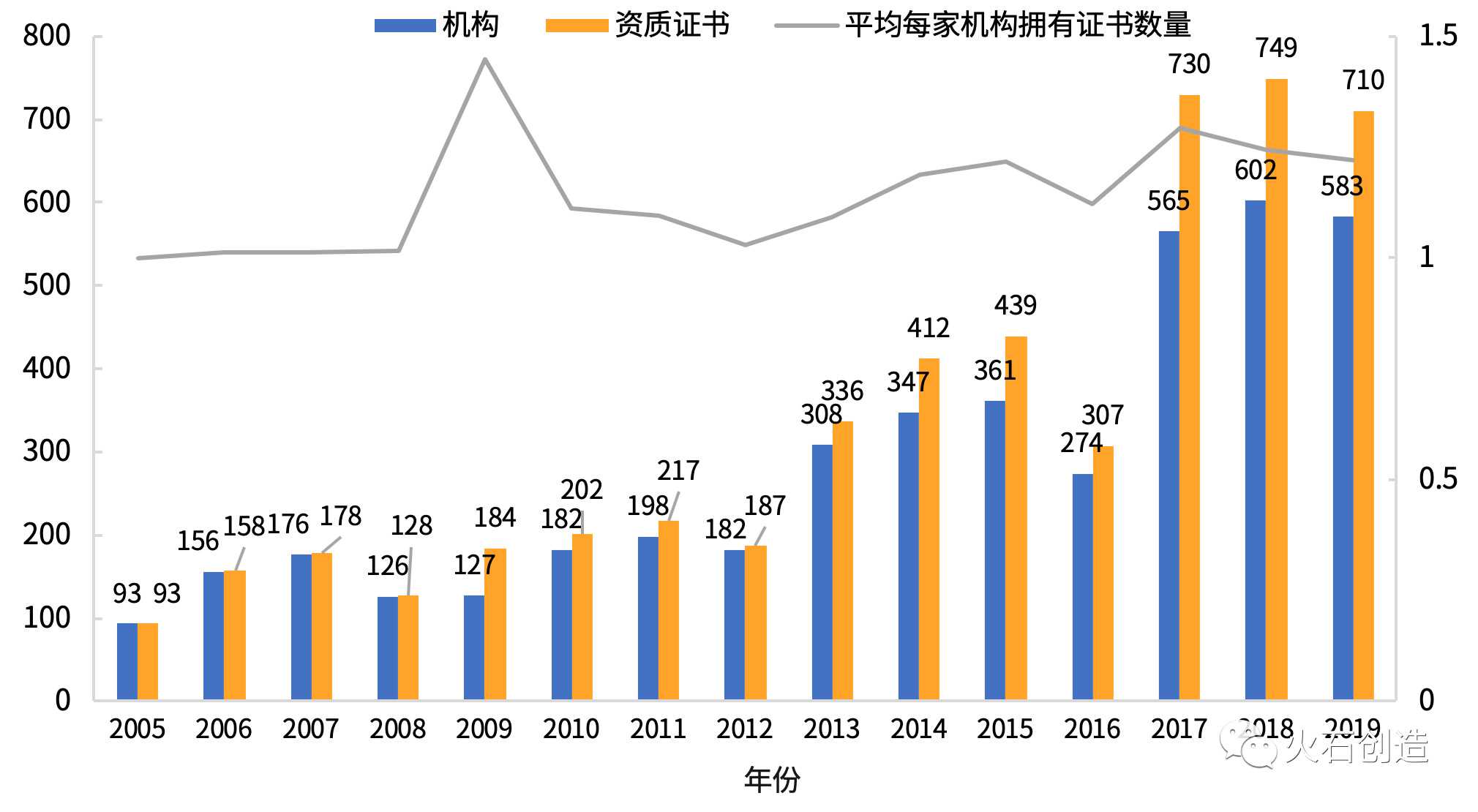
图1 2005-2019年药物临床试验机构数量
注:机构数按当年12月31日持有效资质证书的医疗机构数统计,而不是相加或累加。
其中,根据药物临床试验注册及信息公示平台统计,2016年至2019年约有17%的机构无临床试验注册数据,其中仅17%的机构承担过国际多中心临床试验。
二、我国药物临床试验机构的空间分布情况
1.粤京苏位列前三,粤苏鲁豫川排名提升
从我国药物临床试验机构的省级分布来看,广东、北京、江苏获得认可的临床试验机构数量位居前三,占全国的25% (143/583)。前10位省份的临床试验机构数量占61%(356/583)。
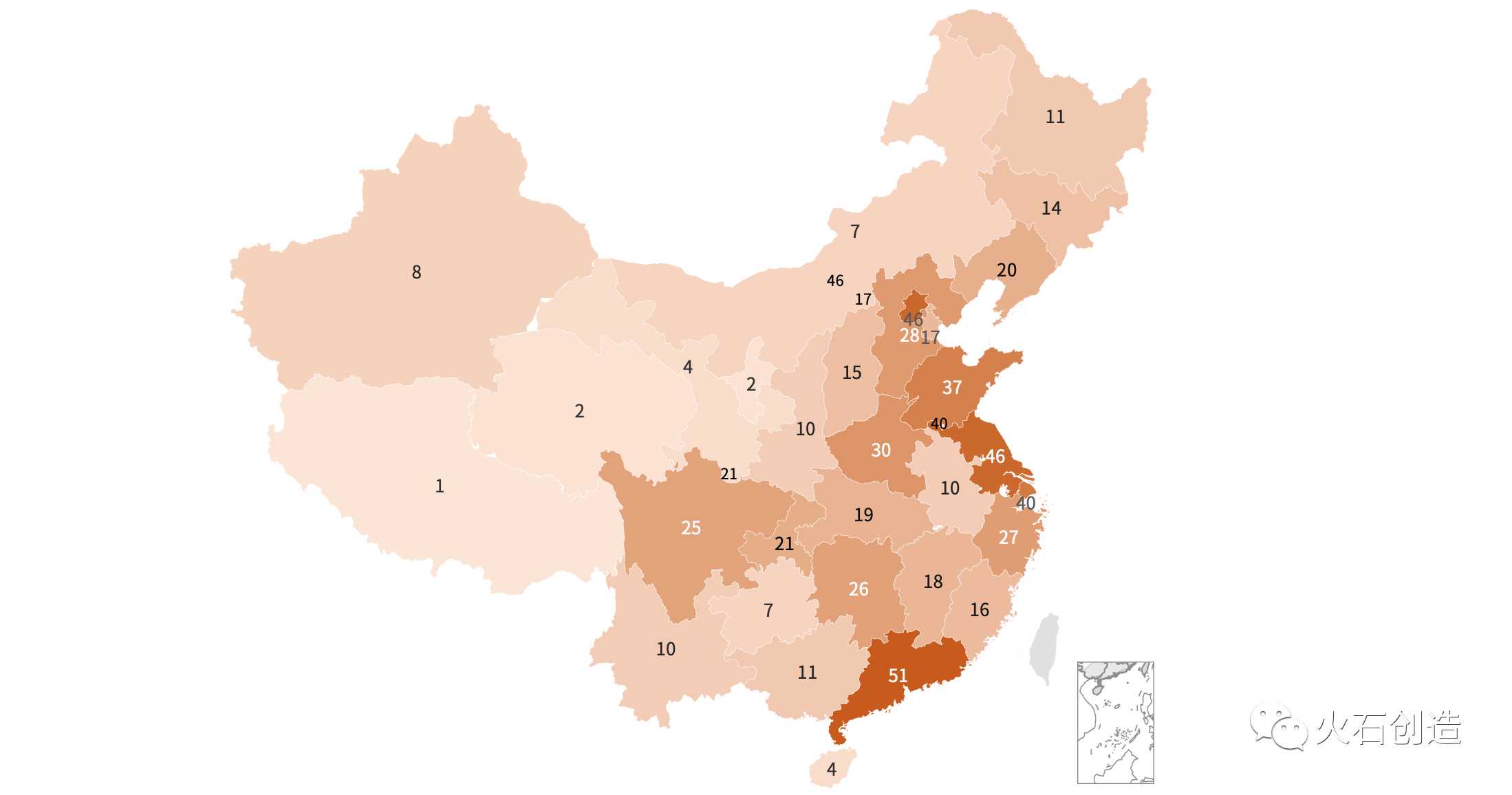
图2中国药物临床试验机构分布
从全国药物临床试验机构省级排名变化趋势来看,2013-2019年,广东、江苏、山东、河南、四川等省市的临床试验机构排名上升,广东从第二位跃升至第一位,河北、四川、河南跃升至前10位。
表1 2019年中国临床试验机构前10名省级分布

2.临床试验机构仍集中在省会城市,非省会城市占比在提升
从临床试验机构的城市分布来看,2019年省会城市共有361家临床试验机构,占比62%,低于2013年的80%。临床试验机构5个的城市中,省会城市占78%(25/32)。大连、厦门、深圳、苏州、温州、无锡等东部沿海非省会城市也因为医疗资源丰富,拥有一批临床试验机构。
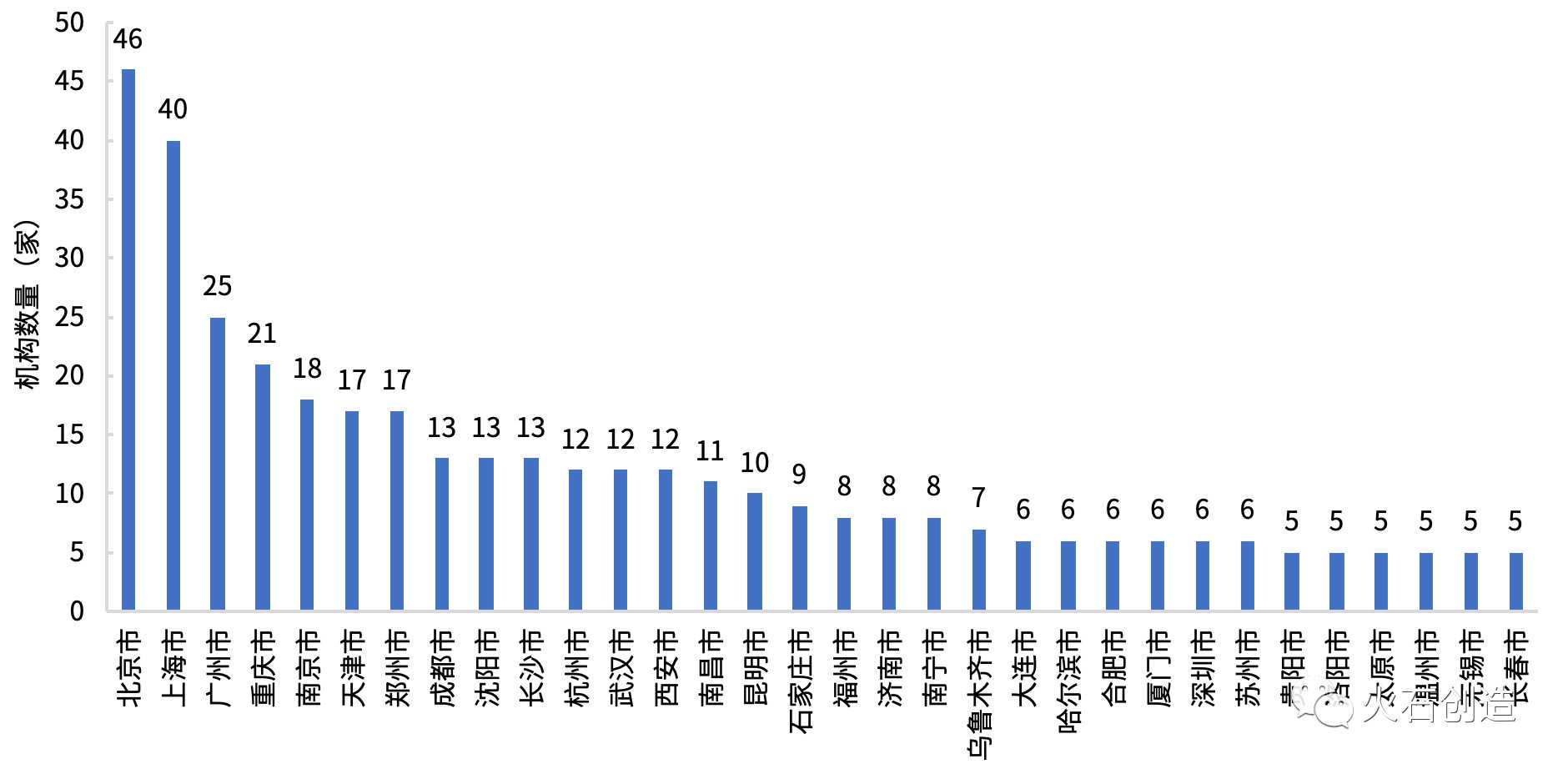
图3中国城市临床试验机构分布
三、我国药物临床试验机构的领域分布
按照我国药物临床试验机构认可的专科分布来看,心血管、呼吸、肿瘤、神经、内分泌五大专科排名第一。作为心血管疾病数量最多、分布最均衡的专业,临床试验机构分布在除西藏以外的各省。
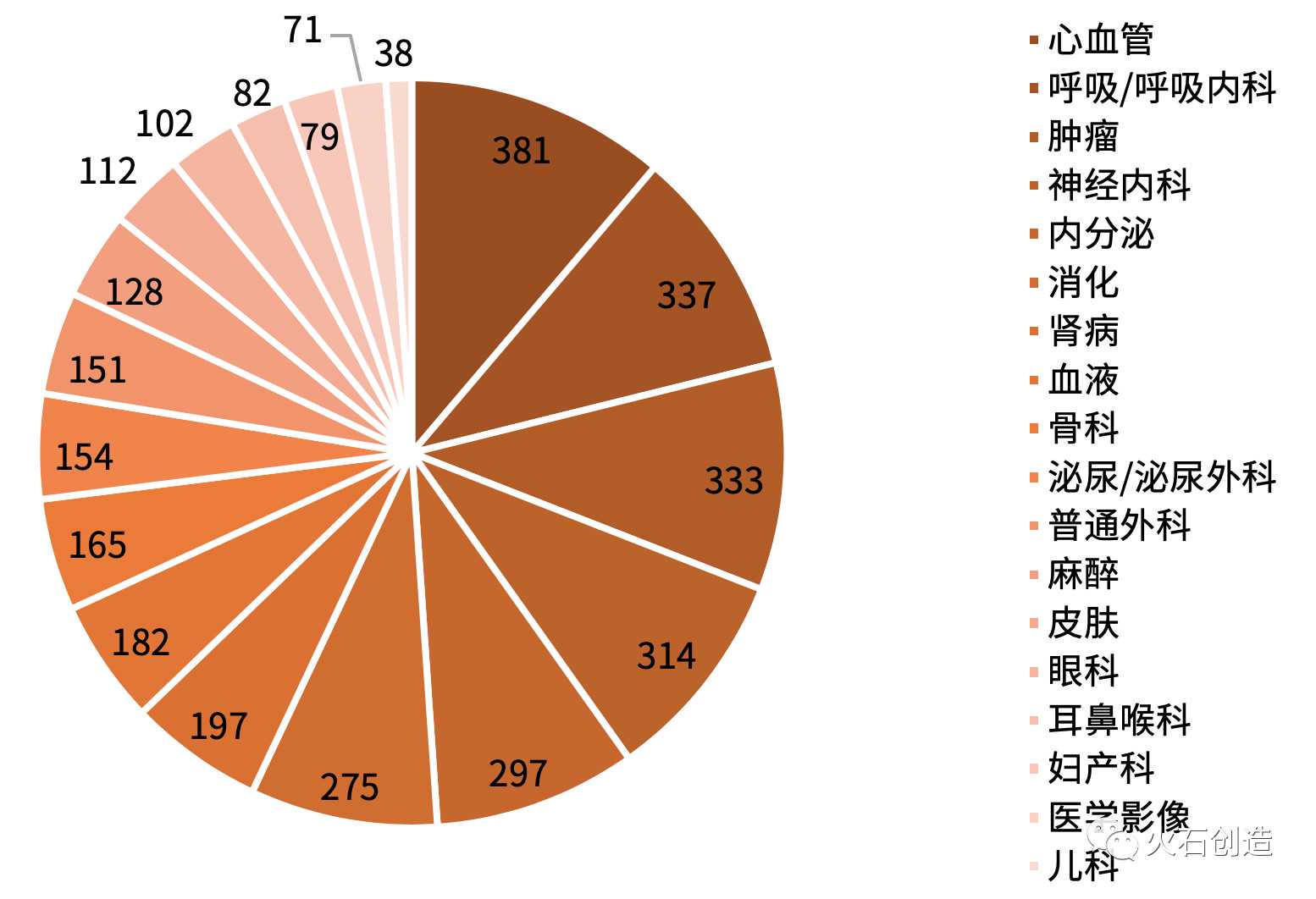
图4中国药物临床试验机构重点专业分布
此外,随着细胞治疗、基因治疗等新兴领域的快速发展,截至2019年8月底,全国已有115家研究机构(含军队医院)通过干细胞临床研究机构备案。其中,北京、广东、上海的注册研究机构数量仍处于领先地位,山东、浙江、云南、湖北、江苏紧随其后。
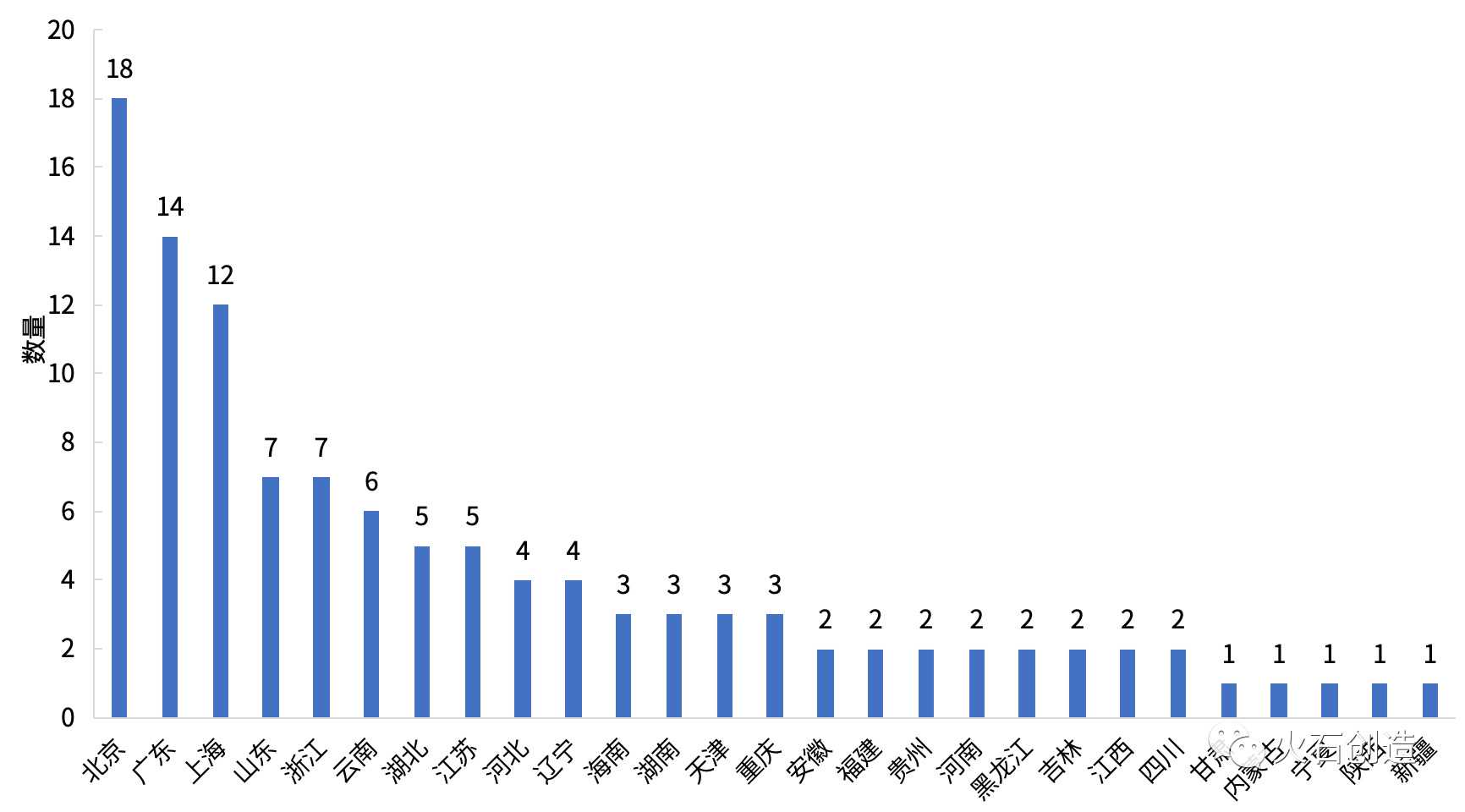
图5中国不同地区干细胞临床研究机构分布记录。
四、我国药物临床试验机构存在的问题及改进建议
(一)存在的问题
目前,在国家鼓励创新政策的推动下,我国药物R&D创新正在加速,药物临床试验机构存在认可数量不足、区域分布不平衡、临床研究资源供需不平衡等问题。
1.药物临床试验机构认定数量不足
根据国家卫生和健康部发布的统计数据
相对于医院总数,临床试验机构的数量应该还有较大的增长空间。随着各级医院基础设施的进一步完善和人员素质的进一步提高,应鼓励有条件的医院申请临床试验机构认可。
2.药物临床试验机构数量地区分布不均衡,与医药研发生产企业不匹配。
从地区分布来看,我国药物临床试验机构主要分布在广东、北京、上海、江苏、浙江等经济发达地区。且集中在省会城市,各省之间和省市内部分布不均。
从与药物R&D和生产企业的匹配度来看,根据弗林特创造数据库,截至2018年底,我国共有62748家生物医药R&D和生产企业,平均108家企业对应1家药物临床试验机构。
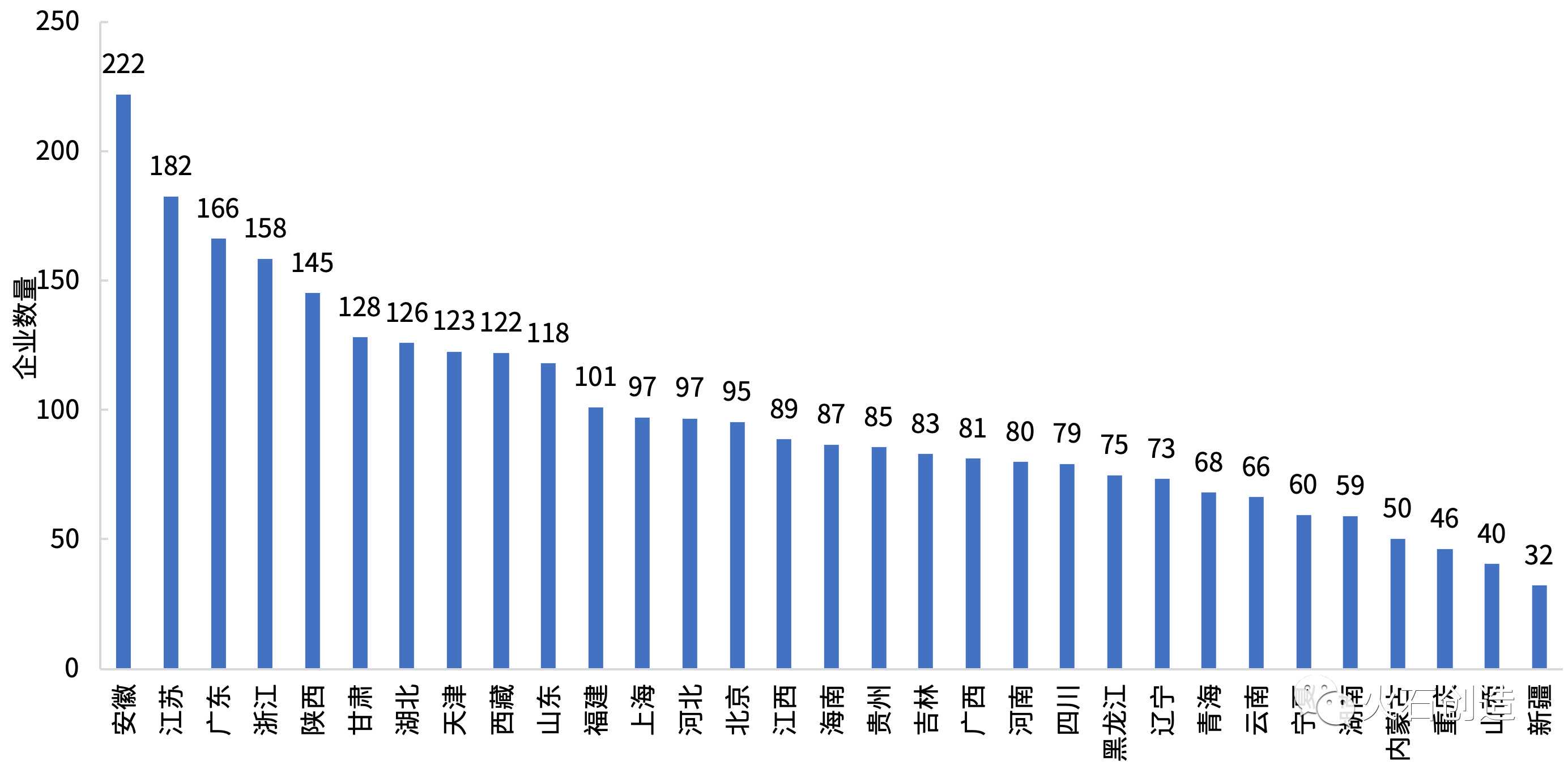
图7中国各地区临床试验机构对应的生物R&D及生产企业数量。
3.临床研究资源供求不均衡
随着创新药物研发的加速,大量药物即将进入临床试验阶段。相对而言,获得认证的临床试验机构数量的年增幅并不明显,临床研究资源的供需失衡问题日益突出。
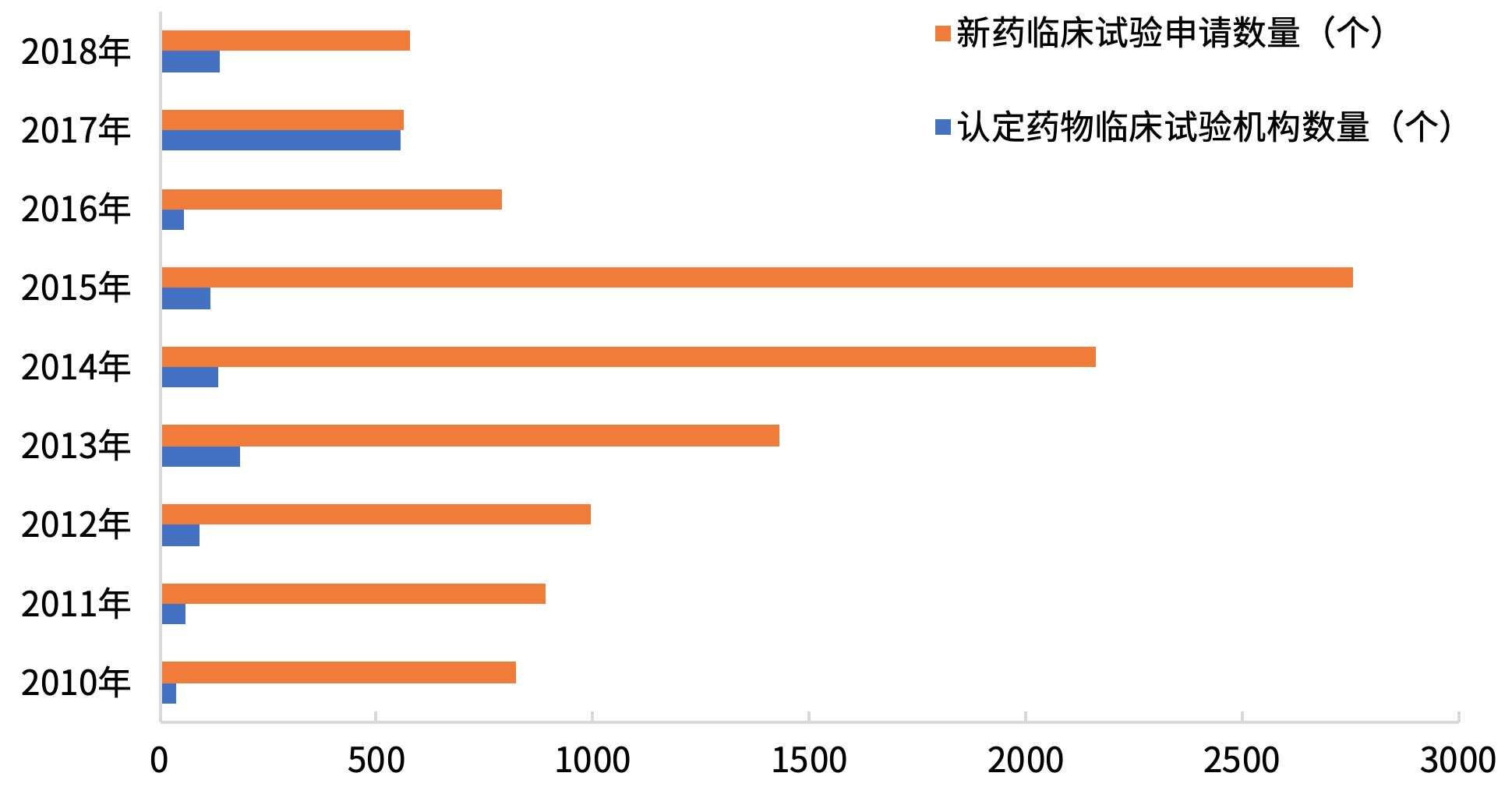
图8我国每年药物临床试验机构数量与新药临床试验申请数量对比。
注:认定的药物临床试验机构数量包括认证期已过的补充申请,不是新数量。
(二)改进建议
1.增加临床试验机构资源供给
随着全球新药研发的进一步加快,新药临床试验,尤其是多中心临床试验将会越来越多的开展。一方面,我国应加快实施药物临床试验机构备案制;另一方面,应鼓励医疗机构开展临床试验,增加临床试验机构的资源供给,以满足越来越多的临床试验需求。
2.建设临床资源服务平台,实现临床试验机构资源整合。
构建开放共享的数字化临床资源服务平台,统筹GCP临床资源,建设世界领先的临床试验I、II、III和真实世界研究能力,建设临床研究服务中心。
参考资料:
[1]张,邹.中国药物临床试验机构的地理和专业分布[J].中国药学,2014 (25): 3471-3474。
[2]绿色篮子。新药文章:十年趋势综述。2018年申请量再创新高[EB/OL].