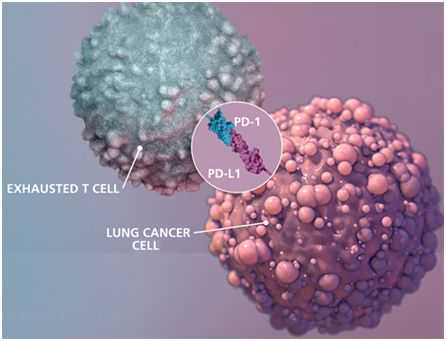
图片来自迈克尔科诺莫斯/埃默里大学医学院。
阻断PD-1通路的抗癌药物(也称为免疫检查点抑制剂)现已被美国美国食品药品监督管理局(FDA)批准用于治疗黑色素瘤、肺癌和其他几种癌症。这些药物通常被描述为在功能失调的T细胞表面“释放刹车”。
在一项新的研究中,来自埃默里大学医学院埃默里疫苗中心和Winship癌症研究所的研究人员证实,即使施加在PD-1上的刹车被释放,这些肿瘤特异性T细胞仍然需要“燃料”进行增殖和恢复有效的免疫反应。这种燃料来自基于CD28分子的共刺激。相关研究成果于2017年3月9日在线发表在《科学》杂志上。论文标题为“PD-1拯救衰竭的CD8 T细胞——靶向治疗依赖CD28”。
尽管PD-1靶向药物取得了成功,但许多患者的肿瘤对它们没有反应。这项研究的发现表明,T细胞表面的CD28可能是一种临床生物标志物,可以预测PD-1靶向药物是否有效。此外,对CD28的需求表明,一些患者可能会失去共刺激,这可能有助于指导联合治疗的设计。
论文作者、埃默里疫苗中心主任拉菲艾哈迈德(Rafi Ahmed)博士说,“许多研究都评估了耗尽型CD8 T细胞表面抑制性受体的表达,但趋化共刺激分子并不是主要焦点。”
Ahmed补充说,“我们最近发现了干细胞样T细胞的一个子集,可以通过PD-1靶向治疗重新激活。现在,我们已经证实,除了PD-1阻断,这些T细胞还需要增殖和分化为基于CD28共刺激信号的杀伤T细胞。我们认为,杀伤T细胞数量的增加对成功免疫疗法的发展很重要。”
在这项新的研究中,这些研究人员首先在小鼠中进行了实验,结果证实,阻断CD28与其伴侣B7之间相互作用的抗体,或者CD28基因的删除,将阻止T细胞在PD-1试剂的反应中增殖。为了评估这些发现对癌症免疫治疗的重要性,这些研究人员分析了接受PD-1阻断药物的肺癌患者的样本。
他们监测了这些患者血液中T细胞的反应,发现大多数CD8 T细胞在PD-1阻断治疗后表达CD28。然而,在早期肺癌患者的活检标本中,肿瘤浸润性CD8 T细胞中CD28阳性T细胞的比例是可变的,从20%到90%不等。Ahmed说,这些结果表明,在PD-1靶向治疗后,只有一部分肿瘤特异性CD8 T细胞会增殖。
论文的第一作者、艾哈迈德实验室的研究人员Alice Kamphorst博士说:“我们观察到,许多浸润性PD-1阳性CD8 T细胞在肺癌患者的肿瘤中不表达CD28。因此,根据我们在小鼠身上实验得到的数据,当PD-1通路被阻断时,这些CD28阴性的CD8 T细胞可能不会增殖。”
她补充说,对CD28共刺激的需求表明,在这些T细胞附近为CD28提供伴侣分子B7的抗原呈递细胞发挥了重要作用,因为B7不存在于大多数肿瘤细胞的表面。
现在,这些研究人员正在研究肿瘤特异性T细胞表面的CD28水平是否可以预测肺癌患者对PD-1靶向药物的反应强度或这些患者的生存期。
Winship癌症研究所副主任Suresh Ramalingam博士说:“我们的研究为评估CD28是否可以作为预测性生物标志物为癌症患者选择免疫检查点抑制剂奠定了基础,也为开发可能提高免疫检查点抑制剂疗效的联合疗法铺平了道路。我们正在Winship癌症研究所进行临床研究,以验证我们在肺癌和其他癌症患者中的发现。”
本文来自生物谷。更多信息,请下载生物谷APP()