今天,美国FDA已经扩大了罗氏药物Zelboraf(vemurafenib)的适应症,以治疗患有血液肿瘤罕见的Erdheim-Chester病(ECD)的成年患者,这是FDA批准的第一种ECD治疗方法。

ECD是一种起源于骨髓且生长缓慢的血液肿瘤。ECD可以增加组织细胞(一种白细胞)的产生,多余的组织细胞可以导致肿瘤侵犯身体的许多器官和组织,包括心脏、肺、大脑等。据估计,ECD影响全世界600至700名患者,并且大约54%的ECD患者具有BRAF V600突变。ECD患者的预期寿命非常有限。这个群体迫切需要新的治疗方法来减轻疾病。
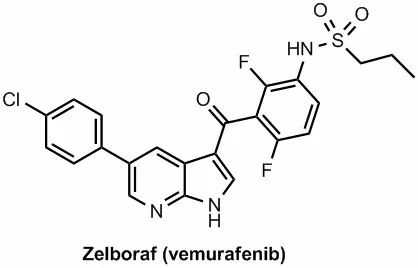
Zelboraf是一种口服小分子激酶抑制剂,可以通过阻断一些促进细胞生长的酶的作用来抑制癌细胞的生长。它于2011年获得FDA批准,用于治疗BRAF V600E突变的不可切除或转移性黑色素瘤患者。由于其抗BRAF V600突变的特性,研究人员认为它也有望用于治疗ECD。针对这一适应症,FDA授予Zelboraf优先审查、突破性治疗和孤儿药资格。
Zelboraf此次获得批准是基于其在VE-BASKET,一项2期研究中的疗效。本试验共纳入22名BRAF-V600突变的ECD患者,并测量了获得完全或部分缓解的患者比例(总缓解率,ORR)。结果显示,接受Zelboraf治疗的患者的ORR达到54.5%,其中11例(50%)获得部分缓解,1例(4.5%)获得完全缓解。使用Zelboraf的ECD患者的常见副作用包括关节痛、斑丘疹、脱发、疲劳等。
“今天,Zelboraf被批准用于ECD患者,这证明了我们可以如何将一些恶性肿瘤的潜在遗传特征的知识应用于其他癌症,”FDA药物评估和研究中心血液学和肿瘤产品办公室代理主任兼FDA肿瘤学卓越中心主任Richard Pazdur博士说。“该产品于2011年首次获得批准,用于治疗一些BRAF V600突变的黑色素瘤患者。现在我们将这种治疗方法带给那些患有罕见癌症但未被批准治疗的患者。”
“FDA的这一决定意味着患有Erdheim-Chester病的患者将首次拥有FDA批准的治疗选择,”罗氏首席医疗官兼全球产品开发负责人Sandra Horning博士说。“我们致力于寻找新的方法,将药物带给需求未得到满足的患者。我们很高兴这项创新的临床试验有助于确定Zelboraf可以治疗这种罕见的疾病。”
ECD全球联盟主席Kathleen Brewer女士说:“这是FDA批准的首个ECD疗法,鼓舞了ECD患者群体,为患者及其家人带来了新的希望。“这种新的治疗方法表明,在患者、家庭、研究医生、行业和FDA的共同作用下,可以迅速取得有意义的突破,以帮助患者。”
我们祝贺罗氏的药物获批扩大适应症,期待它对这一罕见癌症群体的治疗希望!
参考资料:
[1] FDA批准对某些患有Erdheim-Chester病(一种罕见的血癌)的患者进行首次治疗
[2] FDA批准Zelboraf (Vemurafenib)用于BRAF V600突变的Erdheim-Chester病
关注药明康德微信官方账号
