2019年3月20日,罗氏研发的PD-L1单克隆抗体Tecentriq联合化疗(卡铂依托泊苷)获得FDA批准,用于广泛小细胞肺癌的一线治疗,成为近二十年来小细胞肺癌整体生存期改善的唯一突破。
2019年3月28日,PD-1单克隆抗体Keytruda在默沙东的新适应症上市申请获得NMPA批准。培美曲塞联合顺铂用于EGFR和ALK阴性转移性非鳞状细胞非小细胞肺癌(NSCLC)的一线治疗,拉开了我国非小细胞肺癌肿瘤免疫治疗一线用药的序幕。
免疫治疗的优势可以总结为一句话:一旦有反应,部分患者临床治愈,也就是说不复发,不进展,长期存活五年或十年。其中PD-1抑制剂无疑是最好的一种,引领肿瘤免疫的热潮。
作为肺癌死亡人数和发病率最大的肿瘤类型,自然成为PD-1抑制剂的必争之地。一线药物的审批就像电影界的奥斯卡金奖。暗流涌动,刀光剑影,无数失败和传奇在上演。
现在我们来盘点一下PD-1抑制剂最流行的三种单克隆抗体,——Opdivo(简称O药);Keytruda(简称药K);Tecentriq(简称T药)肺癌适应症的批准及未来市场趋势。
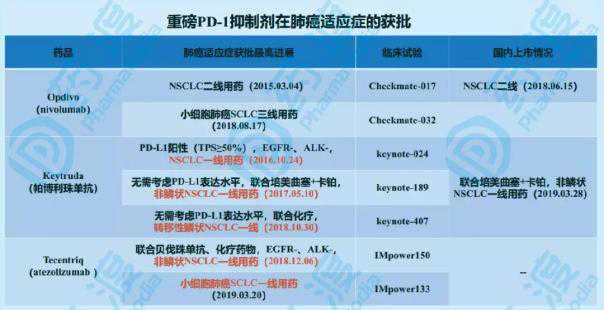
一、非小细胞肺癌(跌宕起伏)
非小细胞肺癌的适应症获得批准。早在2015年3月4日,O药就拿下了二线药,其他适应症差不多,遥遥领先K药,然而K药半年后才进入NSCLC二线用药。一场看似毫无悬念的比赛背后,上演了一场跌宕起伏的大戏。
一线用药和二线用药,虽然只有一字之差,却是天壤之别。只有一线用药失败,才会依次考虑后面的用药方案。一线用药意味着临床使用的优势,代表着对巨大的NSCLC市场的掠夺。
o药立志为NSCLC一线用药,一如既往,踌躇满志,意气风发。checkmate-026三期大规模临床试验如期进行,磨刀霍霍向东沙,结果却是惨淡收场。与标准化疗方案相比,没有明显优势,导致股市动荡。BMS当天股价暴跌,短短几天跌幅高达20%。
与选择PD-L1阳性(TPS > 5%)的非小细胞肺癌患者的药物O不同,默克更加谨慎。药物K选择PD-L1强阳性(TPS > 50%)的NSCLC患者。终于在三期临床试验keynote-024的帮助下,率先为NSCLC服用一线药物,开始显示其王道。
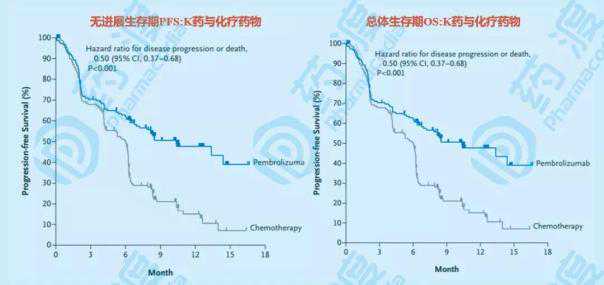
图1:K的药物keynote-024的临床试验数据
当然,默克的野心并不仅限于PD-L1强阳性患者(约占非小细胞肺癌的25%-30%)。它进行了一系列临床试验,以验证PD-L1 > 1%的患者是否能从中受益。NSCLC根据病理特征分为鳞状细胞癌和非鳞状细胞癌。
2017年5月10日,NSCLC的一线药物联合化疗药物获得FDA批准,进一步巩固了NSCLC的霸主地位。在keynote-189临床试验中,在不区分PD-L1表达的情况下,K类药物联合化疗在无进展生存期、总生存期或缓解率方面均取得了明显的临床优势。无论是强阳性TPS50%的患者,还是低阳性TPS的患者,都可以明显从中受益。业内一片哗然。一颗新星从冉冉冉冉升起,在冉冉,非小细胞肺癌的夜空中,闪耀着璀璨的光芒。
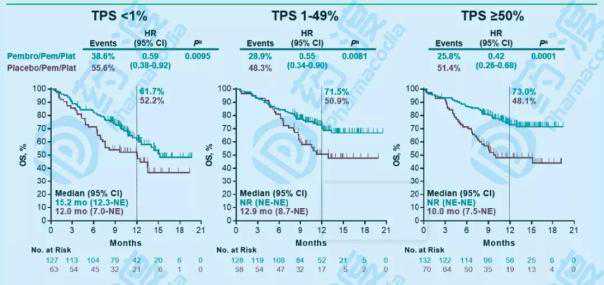
图2:K的药物keynote-189的临床试验数据
2018年6月的ASCO会议上,在医疗圈备受关注的K药以其惊人的临床疗效再次成为全场焦点:三期临床试验keynote-407,无论PD-L1表达(强阳性、阳性、阴性),K药击败标准方案化疗。10月30日,FDA在不考虑PD-L1表达水平的情况下,批准K药联合化疗一线治疗转移性NSCLC(鳞状)患者。
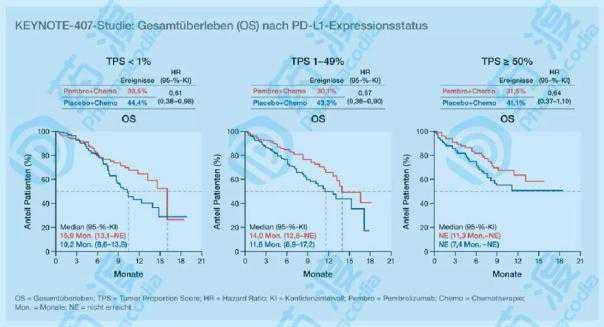
图3:K的药物keynote-407的临床试验数据
k,70%的PD-L1阳性患者服用过,而超过一半的PD-L1阴性患者为非鳞状非小细胞肺癌,也服用过
这个时候BMS的O药在NSCLC好像有点运气不好。在PD-L1生物标志物失败后,人们开始关注肿瘤基因突变负荷TMB。III期临床试验checkmate-227选取TMB大于10,O药物联合CTLA-4单克隆抗体的患者,进行化疗对比,不区分PD-L1阳性和阴性,腺癌和鳞状细胞癌。这是成功的。但由于数据原因,一线NSCLC的审批一再拖延,不仅远远落后于K药,就连罗氏的T药也赶上了。
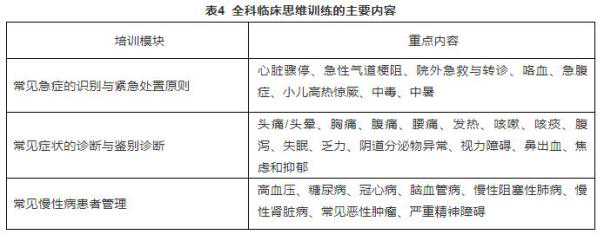
图4:o的药物checkmate-227临床试验数据。
虽然T药直到2016年5月才被FDA批准上市,但拥有广泛肿瘤基础的罗氏,拥有BMS和默沙东不可比拟的行业优势。t药物联合贝伐单抗(我们自己的重磅产品)化疗三联方案,与贝伐单抗化疗相比,是一个III期临床试验进口150;用于晚期非鳞状非小细胞肺癌的一线治疗;第三期临床试验IMpower130是一种结合T-药物化疗、标准化疗和一线治疗晚期肺鳞癌的药物,取得了成功。2018年12月6日,FDA批准T药物联合贝伐单抗和化疗药物用于非鳞状细胞非小细胞肺癌EGFR-和ALK的一线治疗。而同期进行的O药,还在审批环节搁置。真是又苦又撕又闹。
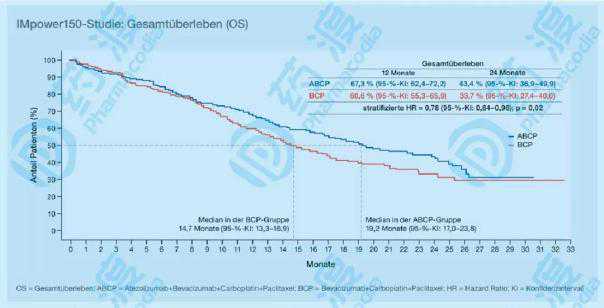
图5:试验药物进口的临床试验数据150
二、小细胞肺癌(喜忧参半)
中小细胞肺癌SCLC约占肺癌病例的15%。与NSCLC相比,SCLC更具攻击性。往往等到癌症进展到晚期才发现患者,临床治疗前景不容乐观。一线药物多为化疗(联合或不联合放疗),但多数患者会在一年内复发。因此,极具挑战性的SCLC也被视为肺癌适应症的最后一片蓝海。
2018年8月17日,FDA基于其在CheckMate-032I/II中的研究成功,批准了用于转移性小细胞肺癌(SCLC)的药物O的三线应用。因此,药物O成为第一个被批准用于治疗小细胞癌的肿瘤免疫药物。这一成功似乎暗示着BMS公司,O药将一扫阴霾,挽救肺癌适应症的下滑。
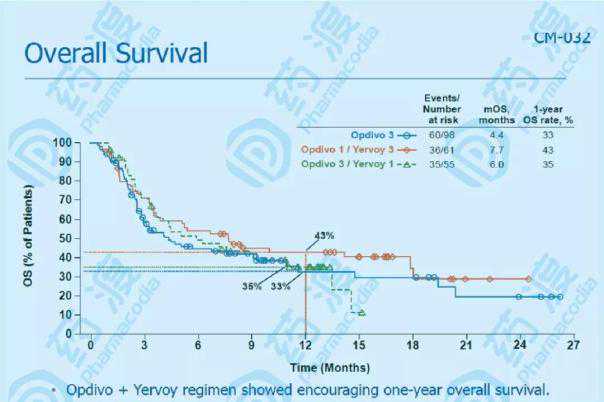
图6:o的药物CheckMate-032临床试验数据。
随着CheckMate-032的巨大成功,BMS加快了SCLC中药物O的大规模III期临床试验的进度,以进一步扩大适应SCLC的批准。似乎过去正在重演。小细胞肺癌二线治疗药物O的期临床试验CheckMate-331和小细胞肺癌维持治疗(一线铂类化疗后)的期临床试验CheckMate-451均以失败告终,总生存期和无进展生存期等重要指标无明显改善。在业内人士看来,这一失败也与BMS对患者生物标志物的选择有关,其招募的患者中肿瘤PD-L1高表达的数量不足。这又一次直接断送了BMS在小细胞肺癌上的苦心优势。
与SCLC中的药物O不同,由于III期临床试验的成功,FDA批准药物T用于联合化疗(卡铂依托泊苷)治疗一线广泛小细胞肺癌(ES-SCLC)的成年患者133。T-drug也是唯一被批准用于ES-SCLC早期治疗的癌症免疫疗法,成为近二十年来SCLC最重大的突破。
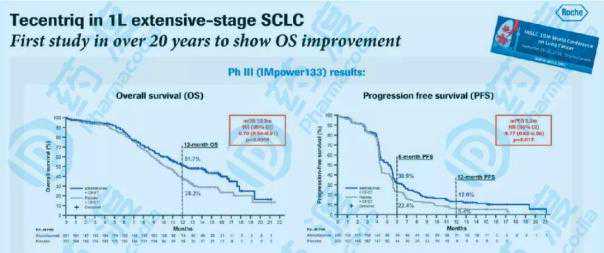
与化疗相比,T-drug化疗方案显著延长了总生存期(中位OS: 12.3个月vs 10.3个月),显著增加了一年OS生存率(51.7% vs 38.2%),显著降低了23%的疾病进展或死亡风险(中位PFS:5.2个月vs 4.3个月),并使一年PFS率翻倍(12.6% vs 12.6%)
总结:从适应症的批准来看,K药在NSCLC的三次大规模临床成功,奠定了NSCLC一线用药的霸主地位。虽然T药一线给药也已获批,但其与贝伐单抗和化疗药物(紫杉醇和卡铂)的三联给药方案在临床使用便利性、疗效和价格优势上并不优于K药,因此难以危机K药的地位。o药物因肺癌适应症审批受阻,未来几年增长会有些乏力。随着
国内市场上,2018年6月,O药NSCLC二线药物获得NMPA批准上市,仅半年时间销售额就将达到4.5亿人民币。然而,K类药物继续保持快速增长趋势。2018年7月25日被批准为黑色素瘤一线药物。只用了5个月就拿下了5亿人民币,初具规模。纳入更大适应症——一线NSCLC后,2019年K药国内销售额不出意外可以轻松突破20亿人民币大关。随着未来几年国产PD-1单克隆抗体被批准用于非小细胞肺癌的适应症,国内免疫时代将进入一个独立政权的时代。