单克隆抗体药物在肿瘤治疗中发挥着不可替代的作用。众所周知的重单克隆抗体赫赛汀仍然是Her2阳性乳腺癌和胃癌转移的主流药物。单克隆抗体杀死肿瘤细胞的能力很大程度上取决于ADCC(抗体依赖性细胞毒性)和ADCP(抗体依赖性细胞吞噬作用)。然而,最近中山大学宋和刘强的研究小组发现,吞噬肿瘤细胞的巨噬细胞(以下简称“巨噬细胞后”)会表达更多的PD-L1和I-DO,从而抑制免疫系统。那么这背后的机制是什么呢?
ADCP后巨噬细胞免疫抑制的具体机制
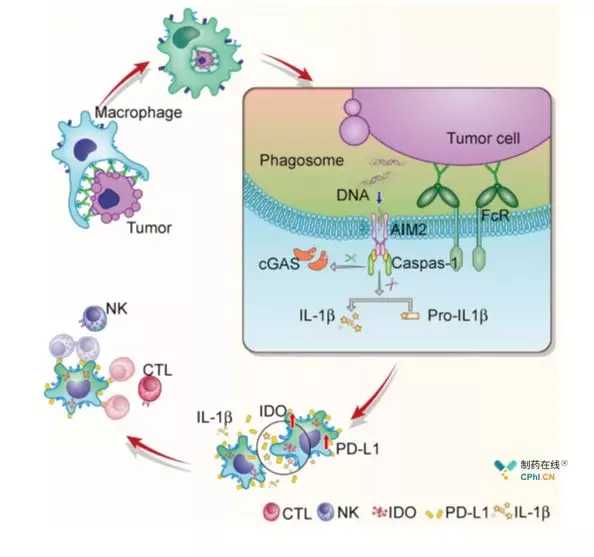
研究人员使用赫赛汀来探索这背后意想不到的机制。当巨噬细胞通过赫赛汀介导的ADCP吞噬肿瘤细胞时,在巨噬细胞内形成含有肿瘤细胞的吞噬细胞,肿瘤细胞分解释放自身的DNA。同时在吞噬细胞的外膜上有一种被FcR募集的DNA感应蛋白AIM2,当DNA穿过吞噬细胞受损的外膜时被AIM2感应,从而激活Caspase-1。活化的Caspase-1催化更多的IL-1前体形成IL-1,最终更多的IL-1导致巨噬细胞产生更多的PD-L1和IDO。PD-L1和PD-1的相互作用抑制T细胞和NK细胞的激活,而IDO导致局部色氨酸缺失,从而停止T细胞的分裂,招募调节性T细胞抑制免疫系统。
赫赛汀与PD-L1抗体和IDO抑制剂联合使用显示更强效果
既然ADCP后巨噬细胞表达更多的PD-L1和IDO,那么同时使用PD-L1抗体和IDO抑制剂会增强赫赛汀的疗效吗?因此,研究人员构建了表达人Her2基因的小鼠(ErbB2),然后接种表达人Her2基因的小鼠乳腺癌细胞,并用不同的药物进行治疗。最后,发现单独或联合使用PD-L1抗体和IDO抑制剂对肿瘤抑制作用仅有轻微影响。但与Her2抗体4D5(赫赛汀的亲本抗体,鼠抗人Her2抗体)联合使用时,PD-L1抗体和IDO抑制剂均表现出明显的抑瘤作用,三者联合使用时抑制作用最为显著。此外,在NSG小鼠肿瘤模型中,当赫赛汀与PD-L1抗体和IDO抑制剂联合使用时,观察到相同的结果。
.jpeg)
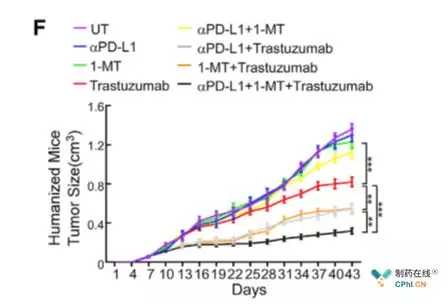
2 Her2抗体(4D5)、PD-L1抗体和IDO抑制剂用于Her人源化小鼠。
在NSG小鼠模型中使用赫赛汀、PD-L1抗体和IDO抑制剂。
既然巨噬细胞在单克隆抗体治疗中起免疫抑制作用,那么如果巨噬细胞不参与单克隆抗体治疗会怎么样?随后,研究员在ERBB 2;这一思路在Csf1op/op(即缺乏Csf1基因的人源化小鼠,其缺乏巨噬细胞)小鼠中进行了探索,发现三者联合并不能增强Her2抗体的疗效,这表明巨噬细胞在三者联合治疗中起着关键作用。
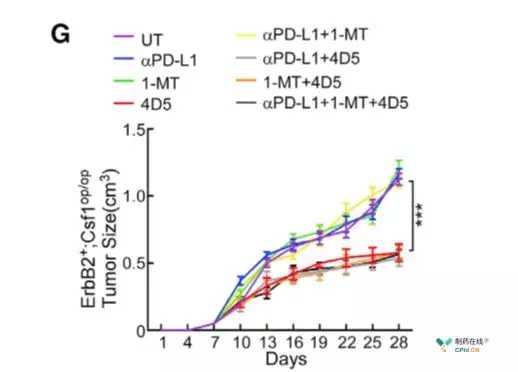
赫赛汀、PD-L1抗体和IDO抑制剂用于巨噬细胞缺失的人源化小鼠模型。
ADCP后巨噬细胞免疫抑制同样存在于人体中
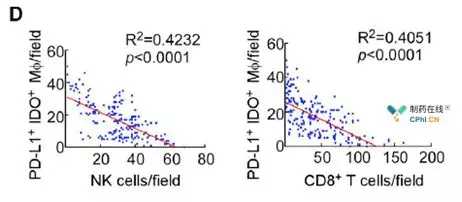
此外,在赫赛汀治疗的Her2阳性乳腺癌组织中,巨噬细胞也表达更多的PD-L1和IDO,而侵袭性NK细胞和CD8 T细胞明显减少,这表明巨噬细胞在人体内ADCP后也会抑制免疫系统,削弱抗体的疗效。
巨噬细胞PD-L1和IDO的表达:NAC w/o T表明只进行化疗,NAC w/t T表明赫赛汀用于辅助治疗。
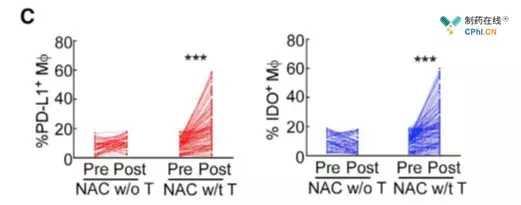
巨噬细胞高表达PD-L1和IDO的肿瘤组织中NK细胞和CD8 T细胞的侵袭
该发现对联合用药的指导意义
巨噬细胞的吞噬作用可以破坏某些肿瘤细胞,在介导适应性免疫反应中发挥重要作用,但这些抑瘤作用可能被PD-L1和IDO高表达引起的免疫抑制抵消,甚至产生不良作用。因此,作者认为该机制可能有助于指导基于抗体的药物的联合策略。比如CD47单克隆抗体可以增强巨噬细胞的吞噬功能,但基于上述机制,或许CD47与PD-1/PD-L1抗体和IDO抑制剂联合应用会有更好的治疗效果。
最后,笔者认为,人体的免疫系统是非常复杂的,肿瘤的免疫逃逸机制也是非常复杂的,所以把这两个复杂的东西结合起来的肿瘤免疫治疗就更加复杂了,所以一方面需要在基础研究上不断努力,尽量把这种复杂的东西搞清楚;另一方面,在考虑治疗方案时,联合用药可能是现阶段更有效的手段。
参考文献:(18) 31179-6,免疫检查点抑制概述了ADCP通过宏诱导的免疫抑制
原标题:细胞牛文:抗体介导的ADCP反而导致免疫抑制,这是新发现或可指导新的联合方案!