2021年上半年,医疗器械产品召回172起,海外产品占大多数。
中国区,3485台
8月6日,国家美国食品药品监督管理局发布《飞利浦金科威(深圳)实业有限公司对心电图机主动召回》,称飞利浦金科威(深圳)实业有限公司报告作为配套产品的锂电池在使用寿命后可能过热或燃烧。飞利浦金科威(深圳)工业有限公司主动召回旗下心电图机。召回等级为二级。
召回的原因是心电图仪使用的锂电池在超过使用寿命后可能会过热或燃烧。因此,当电池的充放电循环次数达到300次,或剩余电池的健康状态(SOH)下降到电池总容量的80%或更低时(以先到者为准),应及时更换。
本次召回主要是对心电图仪软件进行升级,增加了用户提示:当电池充放电循环次数不足或剩余电池的健康状态(SOH)超过可接受的运行极限时,心电图仪会自动提示客户关注电池状态,以便客户及时更换电池。
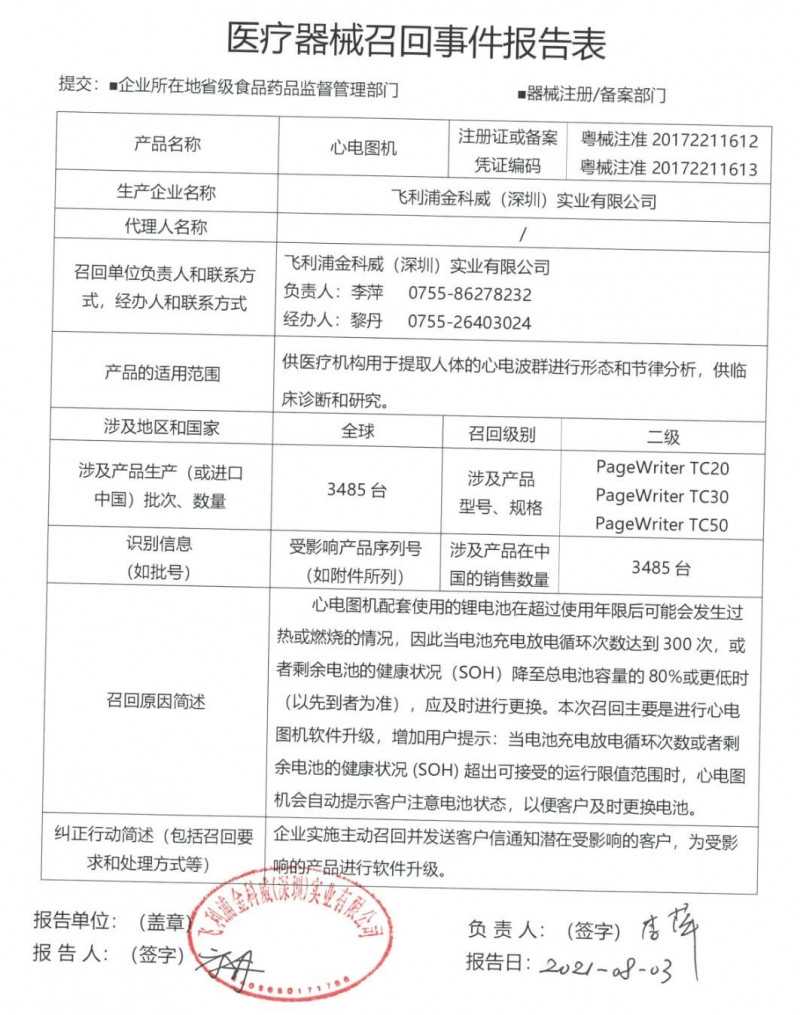
企业主动召回并发送客户信函告知潜在受影响客户,并对受影响产品的软件进行升级。
上半年召回产品境外占84%
根据2017年5月我国正式实施的《医疗器械召回管理办法》(以下简称《办法》),医疗器械召回定义为:
医疗器械生产企业按照规定程序,对已上市销售的某一类别、型号或批次的缺陷医疗器械产品采取警示、检查、修复、重新标识、修改完善说明书、软件更新、更换、撤回、销毁等方式进行处理。
根据医疗器械缺陷的严重程度,医疗器械召回目前分为三个等级。其中,一级召回是指使用可能或者已经造成严重健康危害甚至死亡的医疗器械;二次召回是指医疗器械的使用可能或已经造成暂时或可逆的健康危害;三类召回是指造成危害的可能性较小但仍需召回的医疗器械。
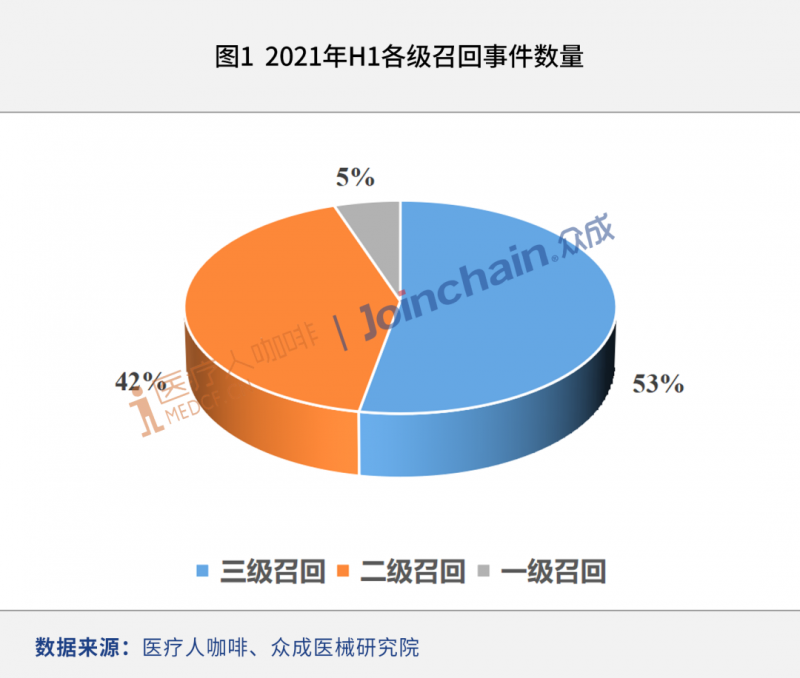
据中诚医疗器械统计,截至6月30日,2021年上半年,国家美国食品药品监督管理局发布产品召回报告172份,涉及医疗器械生产企业119家。三级召回91起,二级召回72起,一级召回9起。
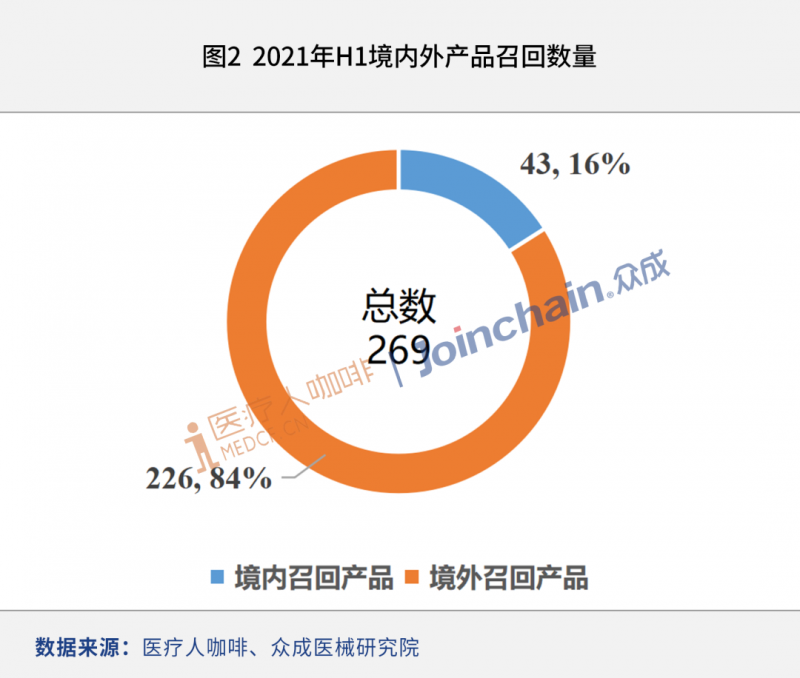
2021年上半年,共有269种医疗器械产品被召回。其中,在中国召回43款产品,占比16%;海外产品召回226种,占84%。从召回产品的分布来看,美国生产的产品有118种,中国有43种,德国有30种,荷兰有23种,英国有13种。
召回原因主要涉及质量问题、标签问题、包装问题和设计问题。
具体来说,产品的指标和参数不达标;产品缺陷会造成安全问题;产品不合格;产品污染;文本错误;包装信息与实物不符;包装的松紧度不符合标准;包装含有异物;包装错误;设计变更有问题。
近期多家械企产品被召回
自8月份以来,美国食品药品监督管理局已经发布了几份召回公告,包括罗氏诊断公司和理邦仪器公司。柏树乐器排列如下: