5日,著名医学杂志《柳叶刀》发表了俄罗斯科学家开发的新冠肺炎疫苗的两项开放标签、非随机1/2期临床试验结果。结果表明,该疫苗表现出良好的安全性和耐受性,有效激发了成年志愿者的抗体和细胞免疫应答。

基于两种腺病毒载体的疫苗设计
该疫苗使用非复制型重组腺病毒载体(rAd)表达新冠肺炎的刺突蛋白(S蛋白)。目前,利用腺病毒载体表达新冠肺炎S蛋白的疫苗设计已应用于新冠肺炎研发的多种疫苗中,康赛诺生物和阿斯利康研发的候选疫苗均已进入三期临床试验,均采用该策略。然而,基于腺病毒载体设计的疫苗面临的一个挑战是,人体的免疫系统不仅会对载体表达的新冠肺炎抗原产生反应,还会对作为载体的腺病毒表面的抗原产生反应。事实上,世界上很多人已经有了针对腺病毒的抗体。
为了减少人体对腺病毒的免疫反应对疫苗效力的影响,这种名为Gam-COVID-Vac的新冠肺炎疫苗使用两种不同血清型的腺病毒载体来表达新冠肺炎的S蛋白。在接种疫苗时,志愿者接种基于血清型26腺病毒载体(rAd26-S)的疫苗,然后间隔21天接受第二剂基于血清型5腺病毒载体(rAd5-S)的疫苗。这种设计和疫苗接种方案有助于降低第二次接种时人体对腺病毒抗原的免疫应答对疫苗效果的影响。
与此同时,研究人员开发了两种剂型的新冠肺炎疫苗,一种是冷冻制剂,另一种是冻干粉。他们在临床试验中测试了这两种配方的效果。
Gam-COVID-Vac的安全性
研究人员进行了两项开放标签、非随机的1/2期临床试验,分别测试冷冻和冻干疫苗的效果。
在1期临床试验中,志愿者接受一剂rAd26-S或rAd5-S疫苗的肌肉注射,并在随后的28天内接受安全性评估。在2期临床试验中,志愿者接受一剂rAd26-S疫苗21天,第一次注射后接受rAd5-S疫苗42天。
研究表明,rAd26-S和rAd5-S疫苗都表现出良好的安全性。研究没有发现严重的不良事件。最常见的不良反应是注射部位发红、低热、头痛、虚弱、肌肉和关节痛。这些症状与以往研究报道的基于腺病毒载体的其他疫苗引起的不良反应相似。
Gam-COVID-Vac的免疫原性
抗体免疫反应
结果显示,在2期临床试验中,85%的参与者在首次接种疫苗后14天产生了针对新冠肺炎s蛋白受体结合域(RBD)的IgG抗体。接种21天后,100%的参与者产生了RBD特异性抗体。在接受第二剂rAd5-S疫苗后,参与者的RBD特异性抗体滴度显著增加。
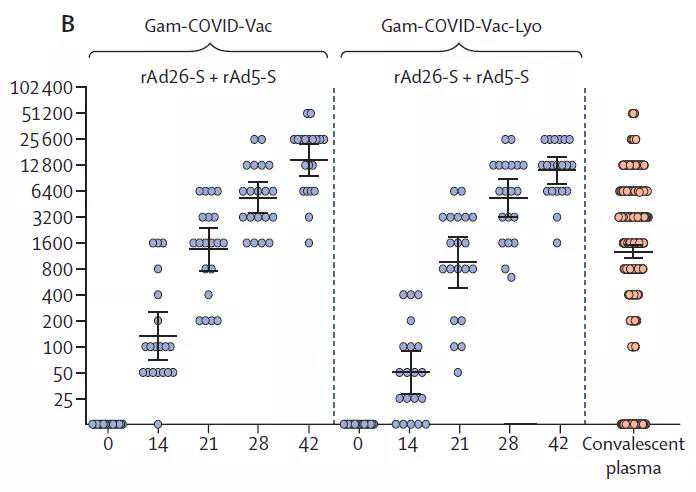
接种疫苗后RBD特异性IgG抗体滴度的变化(Gam-COVID-Vac,冷冻剂型,Gam-COVID-Vac-Lyo,冻干剂型,图片来源,参考文献[1])
人新冠肺炎中和抗体检测结果显示,第一次接种后42天,100%的2期试验参与者产生了抗新冠肺炎的中和抗体,中和抗体水平与新冠肺炎康复患者的平均水平相似。
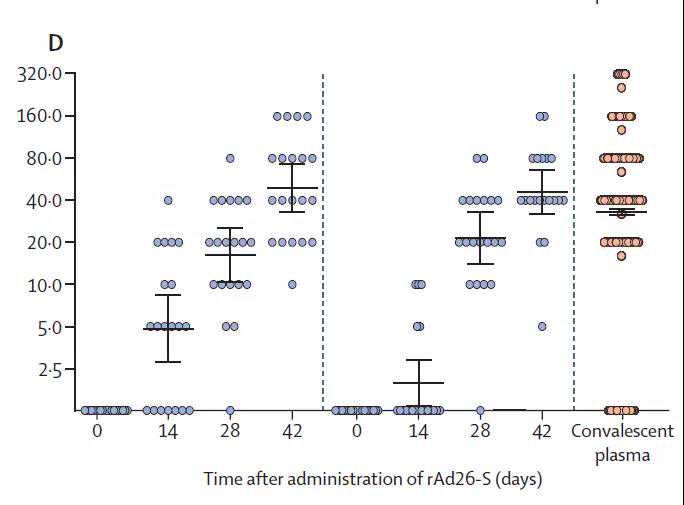
接种疫苗后中和抗体滴度的变化(蓝色数据点为新冠肺炎疫苗两种不同剂型,图片来源:参考文献[1])
细胞免疫反应
研究人员使用三种方法来检测疫苗刺激的细胞免疫反应:血液中新冠肺炎特异性CD4+T细胞的比例,新冠肺炎特异性CD8+T细胞的比例,以及外周血单核细胞释放的干扰素- (IFN-)的水平(IFN-是1型辅助性T细胞免疫反应的生物标志物之一)。结果表明,Gam-COVID-Vac的两种剂型均可显著刺激新冠肺炎特异性CD4阳性和CD8阳性T细胞的增殖和干扰素-的释放。这些结果表明,Gam-COVID-Vac可以有效地刺激参与者的细胞免疫反应。
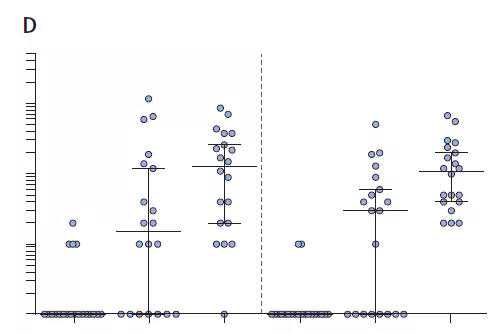
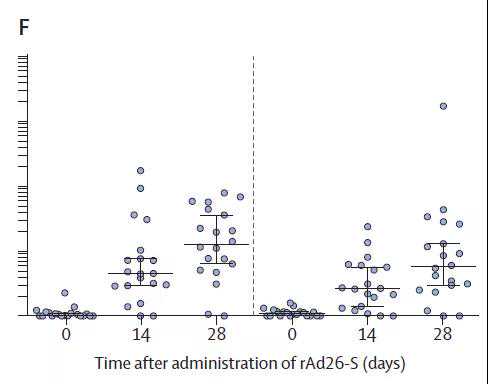
Gam-COVID-Vac能有效刺激CD4+T细胞(B)和CD8+T细胞(D)的增殖和IFN- (F)的释放(图片来源:参考文献[1])
人体对腺病毒载体的免疫反应
由于人体对腺病毒载体的免疫反应可能会影响新冠肺炎疫苗的效力,研究人员测试了参与者针对重组腺病毒(rAd)的中和抗体滴度。结果发现,接种新冠肺炎疫苗28天后,虽然人体会产生针对重组腺病毒的中和抗体,但产生的rAd中和抗体滴度与新冠肺炎受试者产生的RBD抗体和中和抗体滴度无明显相关性,说明对重组腺病毒的免疫反应对新冠肺炎疫苗的效力无明显影响。
此外,接种rAd26-S疫苗后,虽然受试者产生了针对rAd26的中和抗体,但针对rAd5的中和抗体的滴度没有明显增加,这意味着针对rAd26d的中和抗体没有与rAd5发生交叉反应,这可能不会阻碍rAd5的作用。
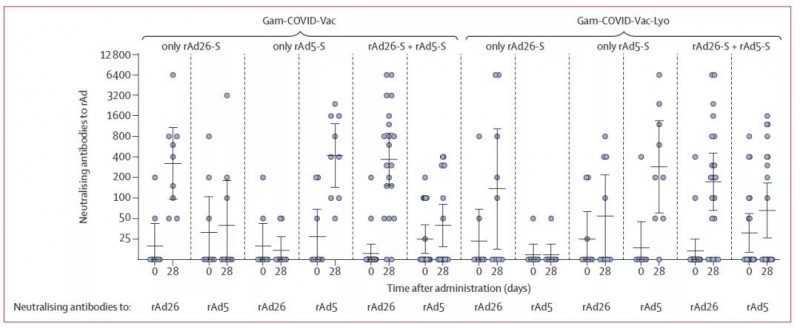
Gam-COVID-Vac接种后受试者抗rAd的中和抗体水平(来源:参考文献[1])
一些讨论
055-79000与此同时,约翰霍普金斯大学的Naor Bar-Zeev教授和Tom Inglesby教授发表了一篇评论。他们说,这项研究有几个优点,其中,冻干粉剂型的开发意味着这种疫苗可以利用世界上现有的冷链技术进行储存和运输。它的稳定性对于保证疫苗能够最大限度地发放到偏远地区非常重要。

但综述也指出,这项研究与其他疫苗候选物的早期研究一样,存在样本量小、随访时间短的缺陷。而且疫苗的免疫原性并不等于对新冠肺炎感染的保护能力,这些特性仍需要大规模的III期临床试验来验证。
而且疫苗的安全性非常重要,因为健康人都接种了疫苗。目前,由于随访时间短,受试者人数少,临床试验中无法发现不常见或罕见的严重不良事件。与疾病治疗的临床试验不同,疫苗的临床试验需要考虑的是疫苗的安全性和人的感染风险之间的平衡,而不是疾病的后果。不安全的疫苗不仅可能对接种疫苗的人造成伤害,更重要的是,可能损害公众对疫苗的信心,导致他们不愿接种疫苗,从而降低他们抵御疾病的能力。因此,本研究中的疫苗与其他候选疫苗一样,最终需要在大规模随机临床试验中证明其安全性和有效性。
参考资料:
[1]洛古诺夫等人,(2020)。两种制剂中基于rAd26和rAd5载体的异源初免-加强新冠肺炎疫苗的安全性和免疫原性:来自俄国的两项开放、非随机阶段研究。柳叶刀,(20)31866-3
[2] Bar-Zeev和Inglesby (2020年)。新冠肺炎疫苗:早期成功和剩余挑战。《柳叶刀》,(20)31867-5
关注药明康德微信官方账号
