文达赵成龙
从2001年开始,陆续批签发了人血白蛋白(麻疹减毒活疫苗、吸附百白破疫苗、脊髓灰质炎减毒活疫苗、乙肝疫苗、皮内注射用卡介苗、人血白蛋白)等6种生物制品。2006年,疫苗和血液制品批签发制度全面实施。目前,我国已将国产血液制品和进口人血白蛋白纳入批签发管理。
目前,我国生物制品批签发工作由CFDA牵头,由中央检验所和7个授权省级药品检验机构(京、沪、粤、甘、川、鄂、吉)共同承担。任务按照生产企业所在辖区进行划分。
2016年,我国共发放血液制品4025批,约5927.8万瓶。虽然近年来我国单采血浆站建设快速推进,但原料血浆供应仍然不足,人血白蛋白存在供应缺口,靠进口人血白蛋白补充。
据火石创建的HSMAP统计,2017年截至目前,已有6个省级药品检验机构公示了所有批签发的血液制品目录(甘肃省和中检院的抽样部分未公开)。在公布的数据中,2017年我国血液制品发放品种有11个,共计3473批次55939625瓶。考虑到此次统计没有包括甘肃省的数据,基本可以推断2010年。
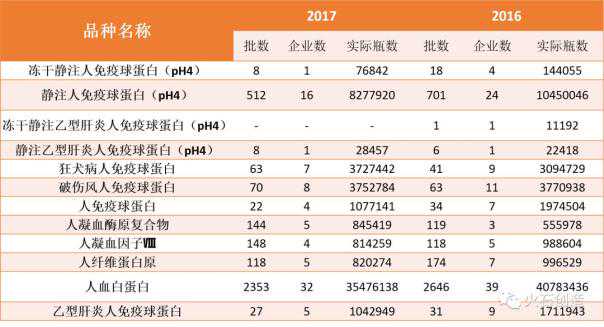
其中,2016年,上海生物制品研究所有限公司生产的冻干静脉注射乙型肝炎人免疫球蛋白(pH4)批11192瓶。今年没有批签发的信息,而静脉注射乙肝人免疫球蛋白(pH4)、狂犬病人免疫球蛋白、人凝血酶原复合物的批签发已经超过去年。
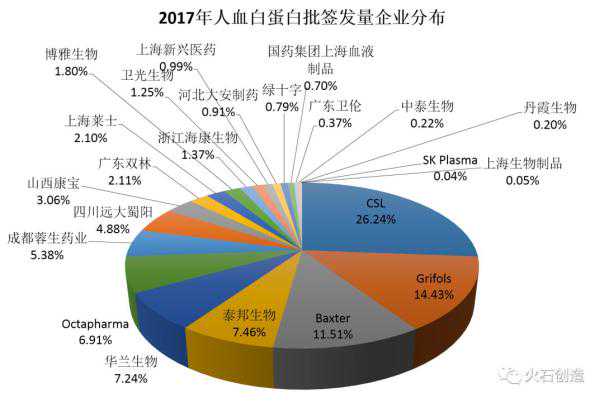
2017年以来,共有32家企业申请获批,其中境内企业22家,境外企业10家。
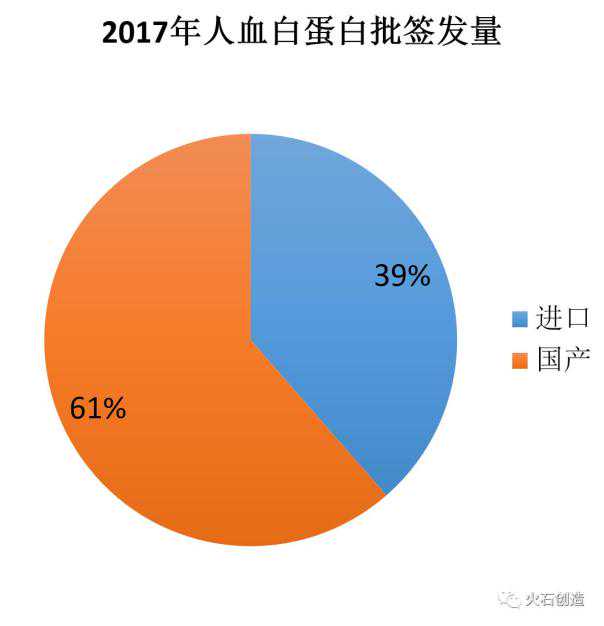
在需要进口以补充供需缺口的人血白蛋白中,2017年进口1057批13486636瓶人血白蛋白,占发放批次的39%,明显低于2016年的56%。
另外,人凝血因子用于血友病的治疗,由于国内市场供应短缺,是血液制品的重点品种。但目前进口人凝血因子尚未纳入批签发体系,按照常规进口产品进行检测。根据这一统计数据,我国已公布人凝血因子产品批签发情况的企业有4家,比2016年减少1家,累计签发国内产品814259瓶,已超过2015年批签发量,但尚未超过2016年。由于这个数据不完整,不能反映全年的真实情况,能否超过2016年还没有定论。
我国血液制品原料长期短缺。随着近年来浆站建设的加快,血液制品的批签发量迅速增加。但2017年上半年数据显示,与2016年同期相比,增长趋势保持了相对稳定的态势。从本次的统计数据可以看出,行业的增长趋势没有明显变化,个别品种的批量发行相对浮动,但对整体影响不大,行业呈现稳定增长态势。至于2017年血液制品的最后一批发放,还是很值得期待的。