2016年,CDE共受理药品注册申请3781件(按受理数量计算,下同),其中化学药品3037件,中药259件,生物制品409件,较2015年分别下降58%、31%和27%。申报的药品数量减半。
CDE近3年受理的药品注册申请

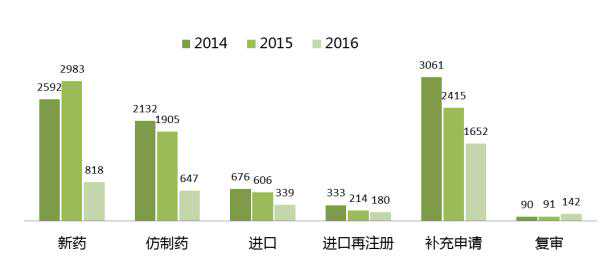
从申报类型来看,除了复审数量增加外,其他申报类型数量大幅萎缩。与2015年相比,新药和仿制药分别下降72.6%和66.0%。
CDE近3年受理的药品注册申请
化学药品
1、旧分类申报逐渐退出舞台
2016年3月4日,CFDA颁布实施《化学药品注册分类改革工作方案的公告》。
7月11日,CDE承接了首个按新药注册分类申报的一类新药——克波美胶囊(法波入华)(见:新药注册分类实施4个月后一类新药申报井喷)。
8月1日,CDE承担了首批三种仿制药——布洛芬注射液(成都远东生物)按新药注册分类申报。
8月8日,CDE承接了四川于慧首批4个仿制药——注射用培美曲塞二钠按照新药注册分类申报(见:新药注册分类落地,各类申报激增)。
自8月份以来,旧的1.1类新药申报已不再出现在CDE,自9月份以来,CDE进行的旧的3.1类新药申报数量急剧下降。因为基数大,老六类申报要淡出历史舞台可能还需要一段时间。
2、1类新药申报升温
自3月化学药品注册新分类实施以来,仿制药(旧6新4)和假药(新3旧3.1)呈断崖式下降,创新药(新1旧1.1)数量总体稳定。
2016年创新药(新1旧1.1)注册申请240件(按受理数量计算),较2015年增长19.4%,共涉及89个品种。其中,报告EGFR抑制剂的公司超过7家,报告PARP抑制剂的公司超过4家。
2016年申报的89个一类新药
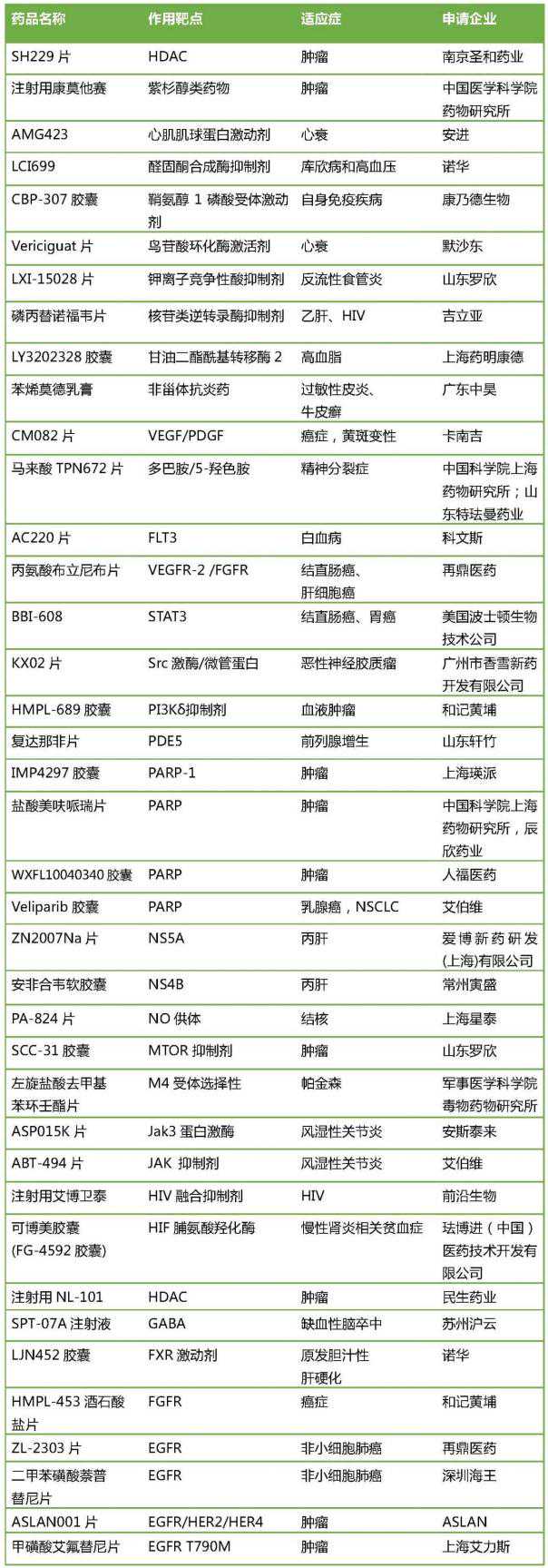

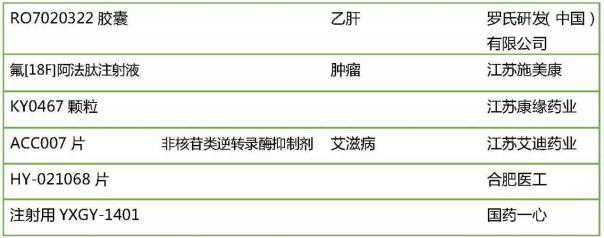
3、仿制药热门申报品种
他达拉非、沙库比曲/缬沙坦是2016年最受欢迎的仿制药申报品种,申报数量超过30个。
2016年申报的仿制药超过20个。
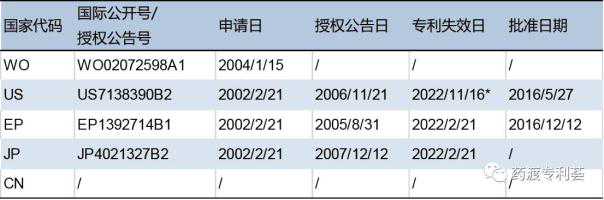
中药、治疗用生物制品
2016年中药申请259件,其中76%为补充申请,仅12%(32件)为新药申请,1类新药无申请。第6类新药(未在国内上市销售的中药和天然药物复方制剂)申请占绝大多数,中药新药创新仍然停滞不前。
2016年治疗用生物制品相关申请319件,其中一类申请活跃,占32%,涉及23个品种。热门目标PD-1/PD-L1的相关申报显示为红色。
2016年中国申报的第一类治疗性生物制品

5家豪门药企注册申报盘点
1、江苏恒瑞
2016年,江苏恒瑞药业有限公司申请乏善可陈,仅有1个6类仿制药(马来酸茚地罗吸入粉雾剂)和1个3.4类新药申请,其余均为补充申请。并且撤回了磷酸瑞格列汀和聚乙二醇重组人粒细胞集落刺激因子注射液(19K)两个重品种的生产申请。
但恒瑞2016年获得的临床批文数量高达40个(按品种分,见:2016年五大巨头药企获得的临床批文),罂粟乙烯碘油注射液和注射用达托霉素两个品种获批上市,收获依然满满。
恒瑞医药2016年提交的注册申请
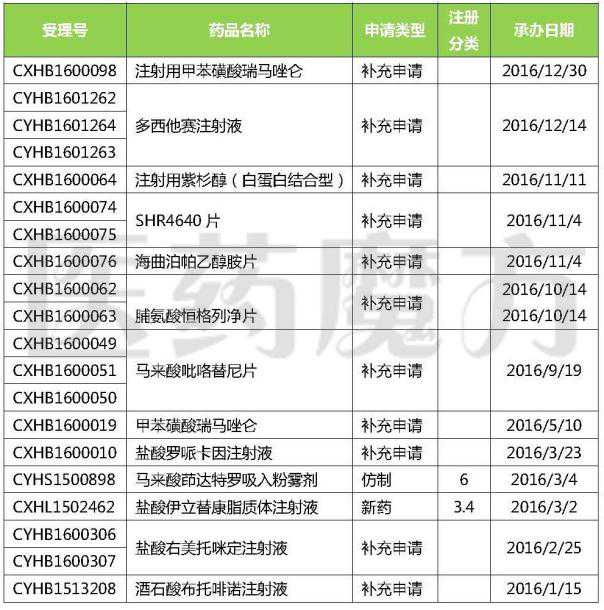
注:仅统计江苏恒瑞。
2、正大天晴
郑达天晴2016年的表现堪称土豪。共申报14个(以受理数为准)一类新药,新药管道迅速扩大。此外,还包括2个2.1类改进新药、23个3.1类新药和1个3.2类新药。唯一的仿制药替诺福韦酯已进入申请生产阶段,被列入优先审评。
注册申请
2016年,海正生物制品和化学药申报双管齐下,有德固胰岛素、甘精胰岛素、达沙替尼片、重组抗RANKL人单克隆抗体注射液等多个重磅品种。审批方面,海正药业2016年共获得35个临床批文(见:2016年五大巨头药企获得的临床批文)。
海政2016年提交的注册申请
3、华海药业
齐鲁制药2016年全方位发展包括1.1个新药WX-0593,6个仿制药,5个修改剂型。第5类申报均为口服可溶性膜剂。国内还没有批准上市的口腔溶膜产品,都在研究中。齐鲁口腔溶膜平台要发力了(见:口腔溶膜制剂国内发展现状宣言)。
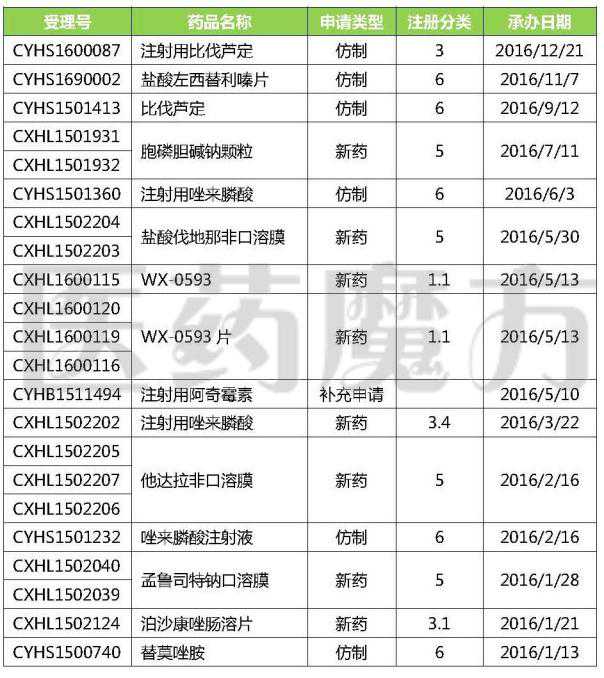
齐鲁2016年提交的注册申请
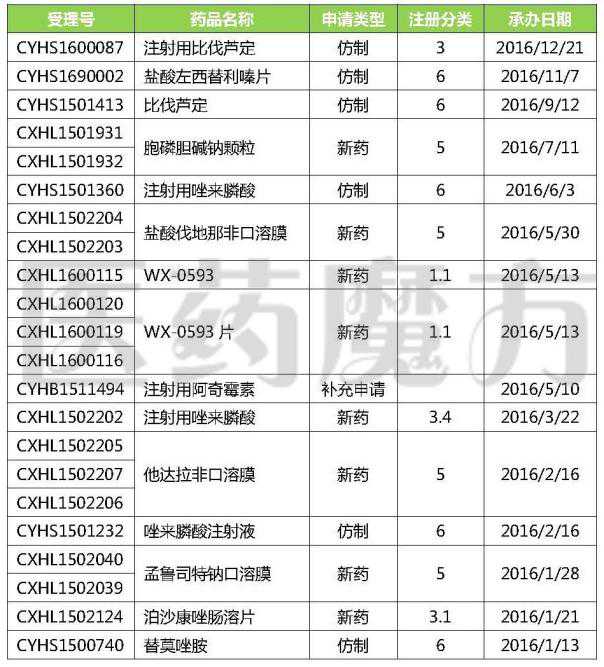
注:仅统计齐鲁制药有限公司